Orrori dalla II prova intercorso

No, non si tratta di un errore nel titolo.
Di seguito sono riportati alcuni degli errori gravissimi fatti nella prova.
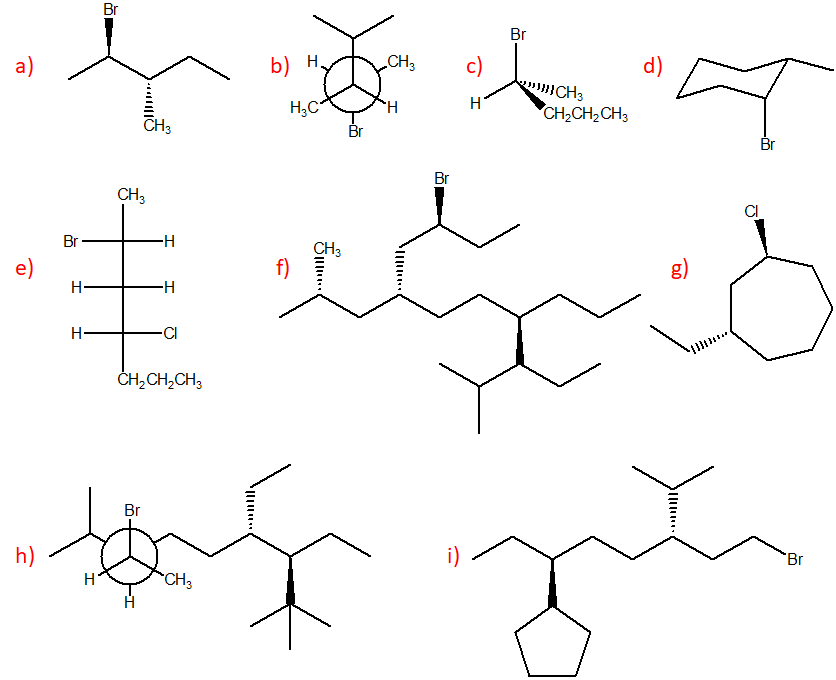
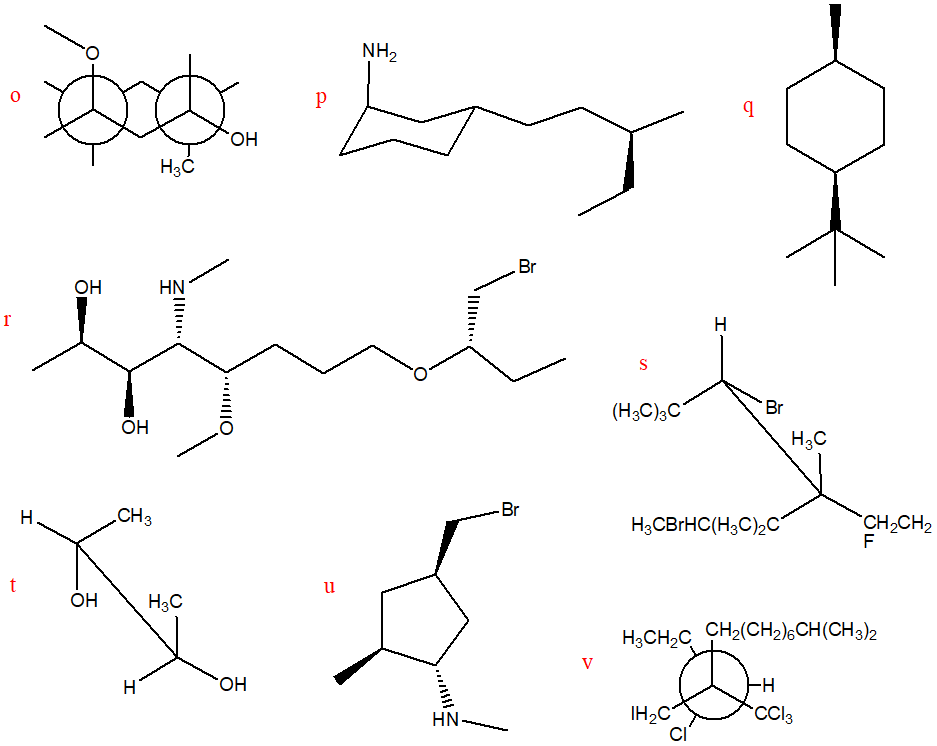
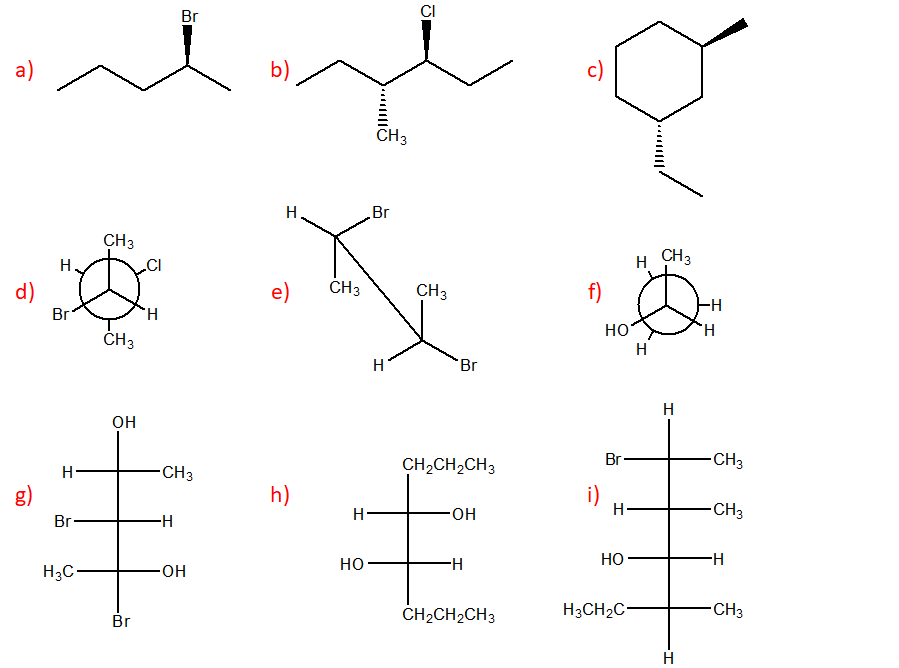
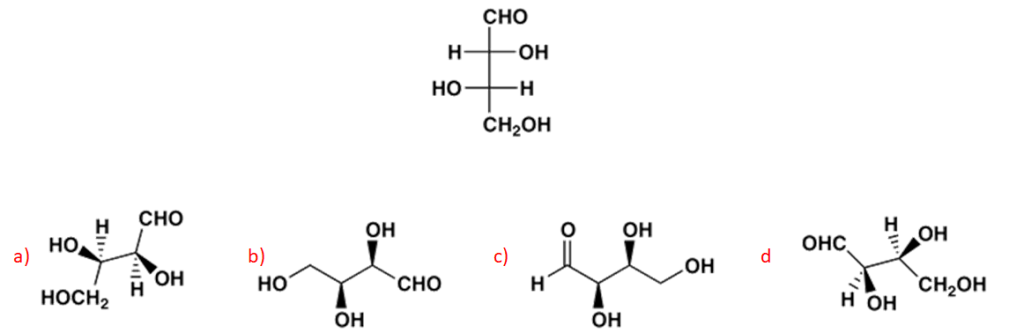
1) Partiamo da quello meno grave, in quanto può essere risolto esercitandosi di più: problemi con l’attribuzione della configurazione assoluta e nelle interconversioni da una rappresentazione all’altra. Si raccomanda di prendere visione anche del materiale didattico presente qui sul blog.
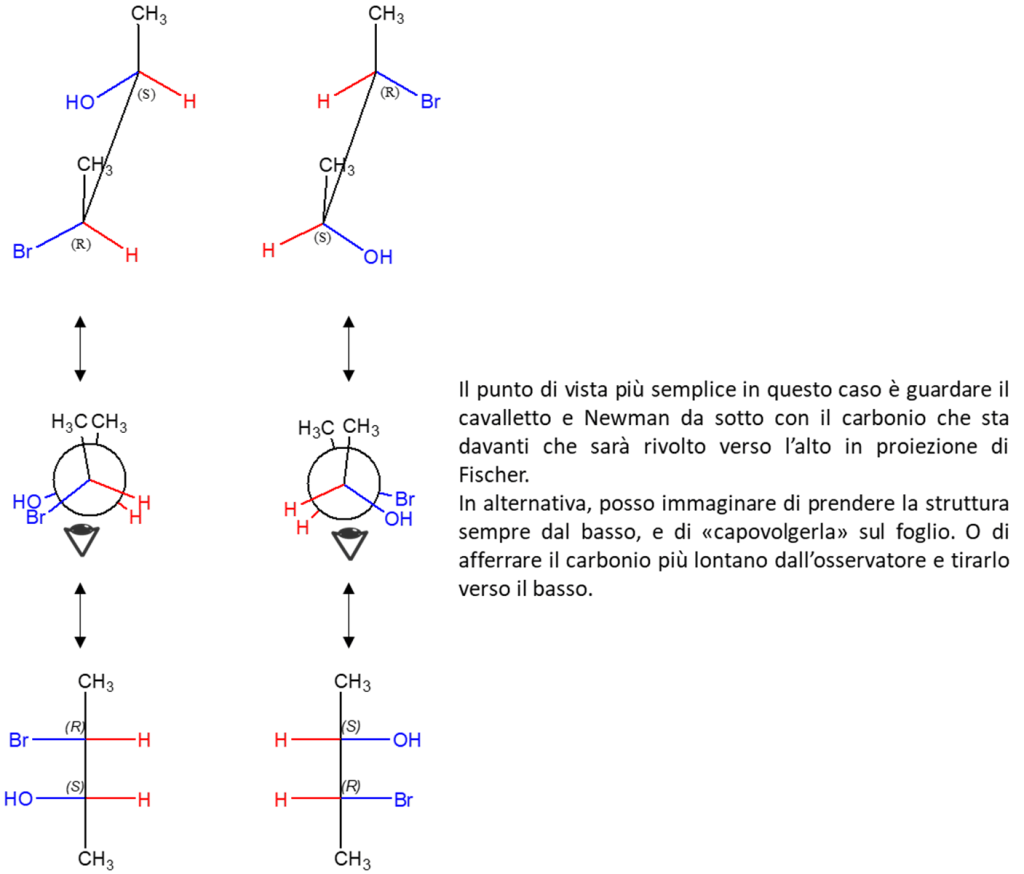
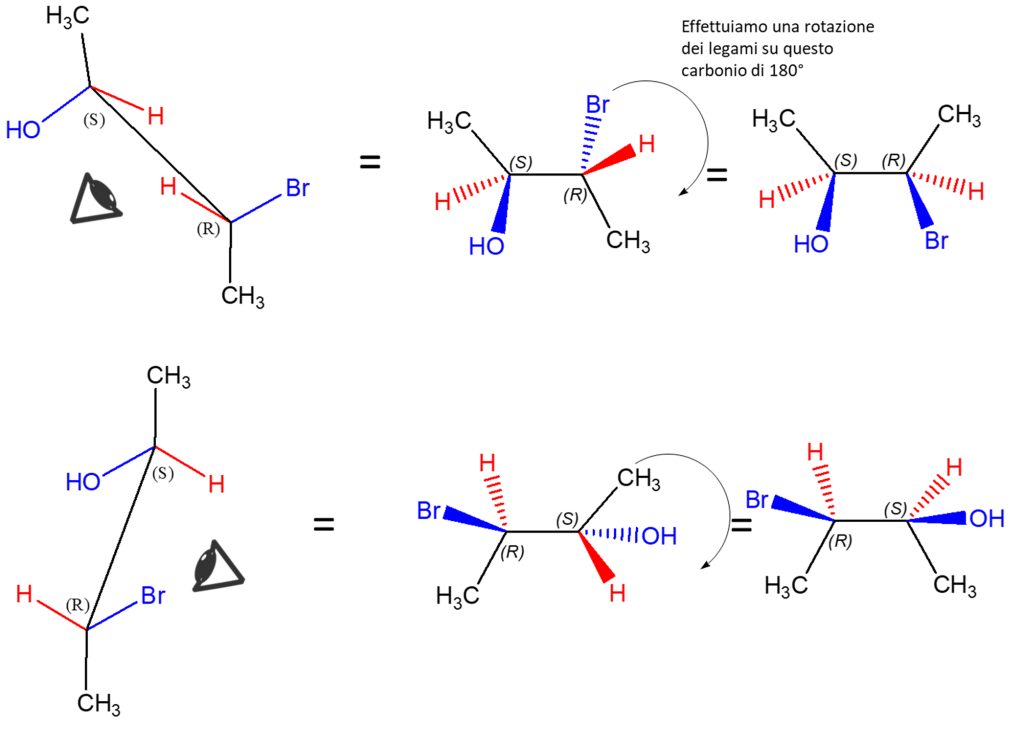
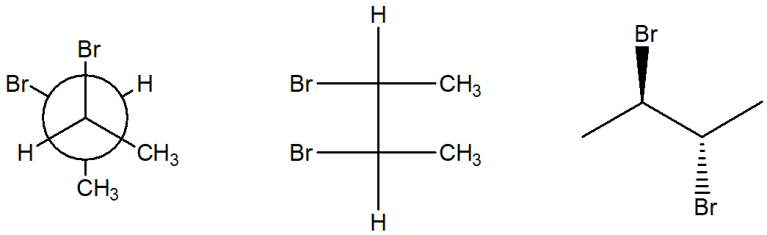
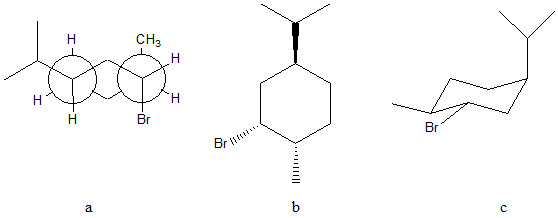
2) L’analisi conformazionale a volte è fatta in maniera confusa e caotica: nello scrivere le varie conformazioni è importante non ruotare mai contemporaneamente entrambi i carboni di una proiezione di Newman. Sceglietene uno e ruotate sempre e solo quello e sempre nella stessa direzione.
3) NON ESISTONO legami equatoriali e assiali in una proiezione di Newman di un composto a catena lineare.
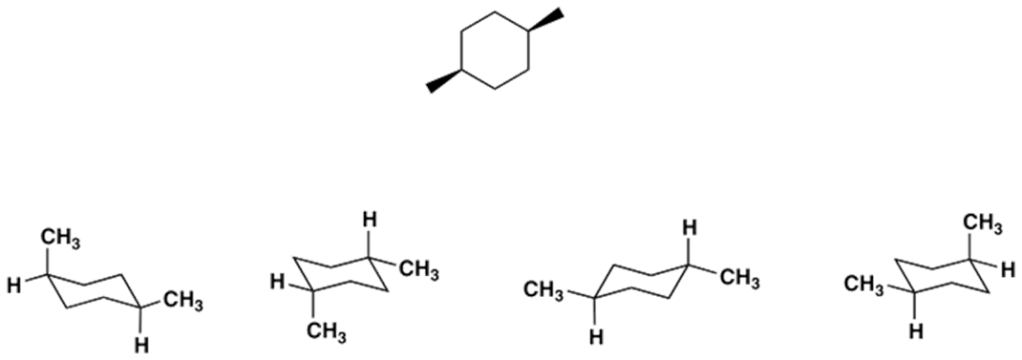
4) Il composto mostrato a sinistra è correttamente rappresentato dalle due sedie a destra. Queste due conformazioni si interconvertono l’una nell’altra (passando attraverso le altre conformazioni del cicloesano). Ne consegue che se devo confrontare una struttura a segmenti con una sedia NON potrò MAI dire che le due strutture sono isomeri conformazionali (in quanto quella a sinistra è rappresentata da entrambe le sedie a destra)
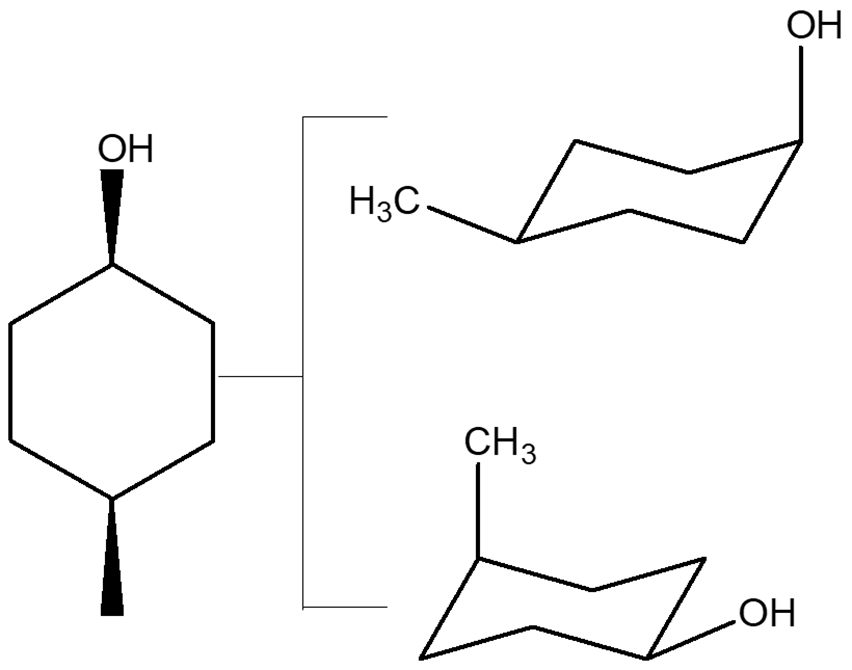
5) Il composto in alto non è chirale, per cui, se lo confronto con qualsiasi altro cicloesano sostituito, questi non potranno essere tra loro isomeri ottici.
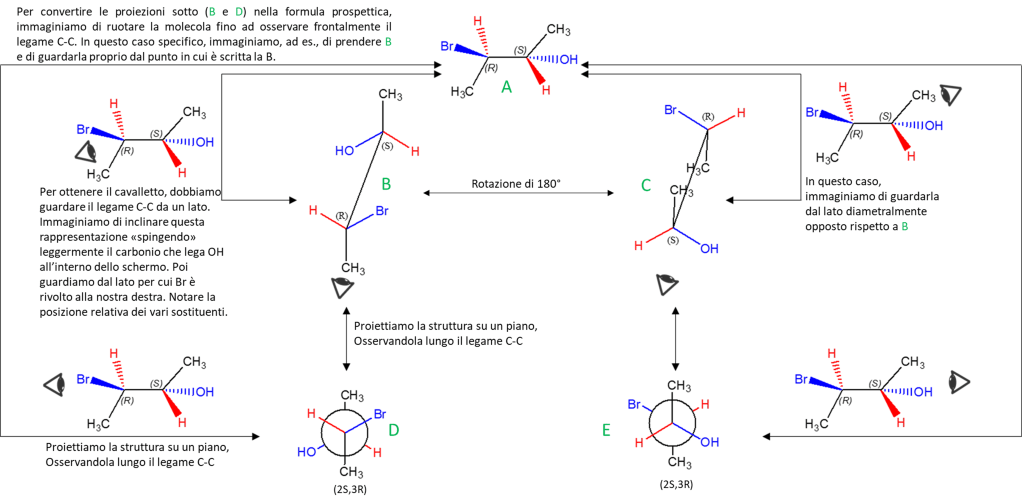
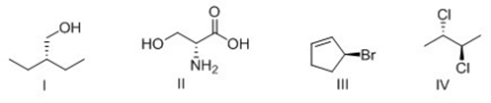
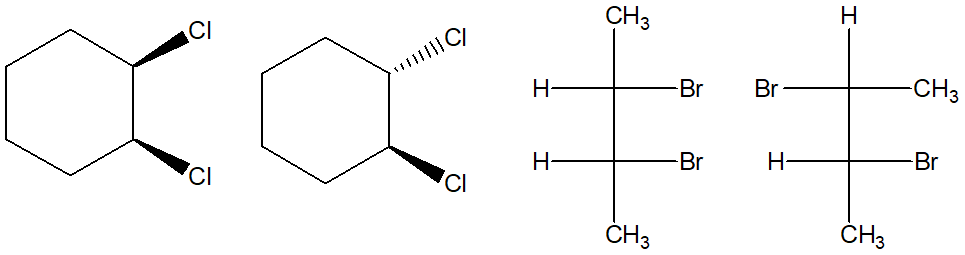
6) S–>R e viceversa. S NON DIVENTA MAI R (e viceversa) ammenochè non rompiamo dei legami e scambiamo dei sostituenti. Il sistema di Cahn-Ingold-Prelog (CIP) ci impone di osservare la molecola in modo da avere il sostituente a priorità minore lontano dall’osservatore. Se questo è rivolto verso l’osservatore, è chiaro che sto guardando la molecola dal lato diametralmente opposto a quello prescritto da CIP, per cui rotazione oraria corrisponderà in questo caso a configurazione assoluta S e antioraria a R
7) Collegato al punto 6, se il sostitutente a priorità minore è sul piano NON POSSO attribuire la configurazione assoluta. E’ NECESSARIO effettuare una rotazione. Data la difficoltà di immaginare questa rotazione, il modo più semplice per attribuire la configurazione assoluta a questo carbonio è: I) fare uno scambio (in questo caso, sì che cambia la configurazione dato che ottengo l’enantiomero del composto iniziale) portando il sostituente a priorità minore lontano dall’osservatore e II) attribuire la configurazione all’enantiomero del composto di partenza. Nota questa, è nota anche quella del composto iniziale.
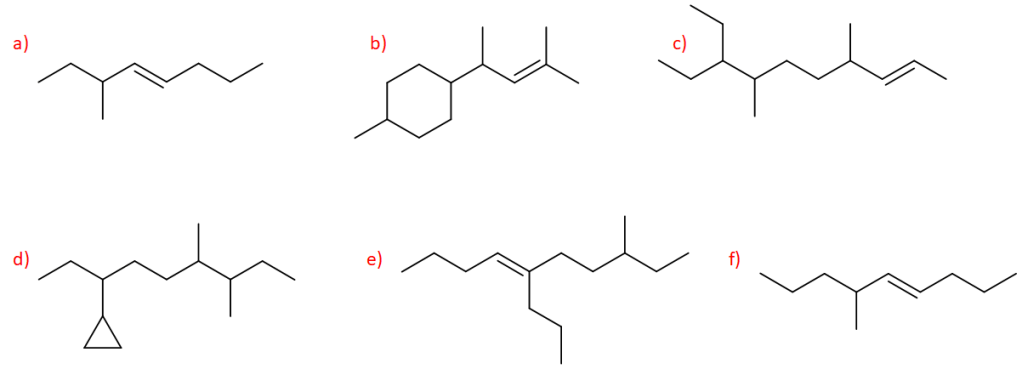
8) Nomenclatura: a) è essenziale usare correttamente virgole, trattini, parentesi, ecc. b) non è possibile dimenticare le regole di nomenclatura (e se questo succede, è il caso di rivederle) ed andare in confusione quando le rappresentazioni strutturali cambiano leggermente. Vediamo due esempi presenti nella prova:
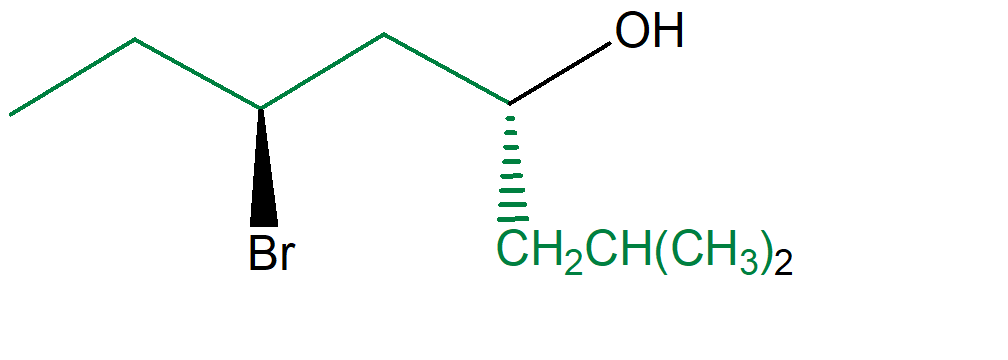
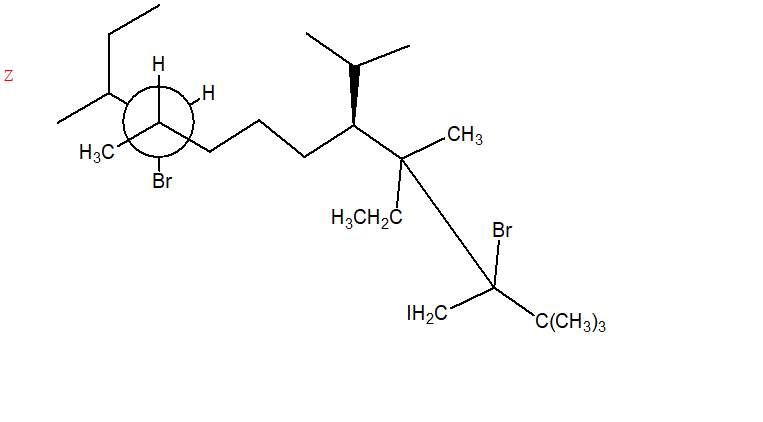
La catena principale è indicata in verde: quella continua più lunga contenente il carbonio che lega il gruppo funzionale. Il carbonio 1 sarà quello presente ad una estremità, e in particolare a quella che mi permette di attribuire il numero più basso possibile al carbonio che lega il gruppo funzionale. Questo composto si chiamerà:
(4R,6S)-6-bromo-2-metil-4-ottanolo.
A seguire un altro esempio (la catena principale è anche qui indicata in verde):
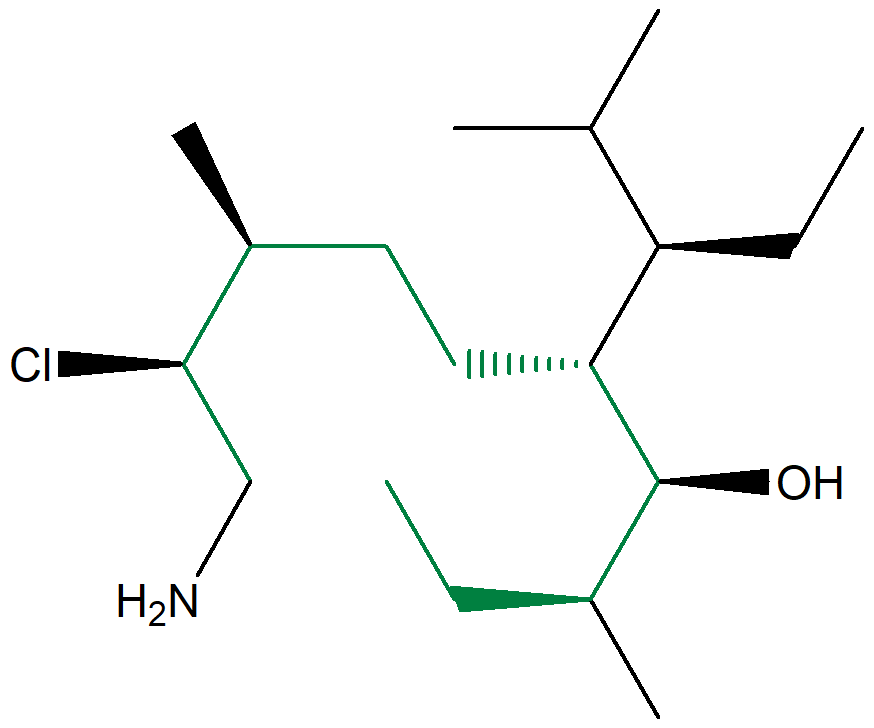
(3S,4S,5R,8S,9S)-10-ammino-9-cloro-5-[(1R)-1-etil-2-metilpropil]-3,8-dimetil-4-decanolo




















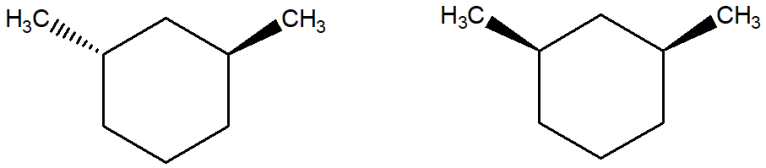








You must be logged in to post a comment.