Calendario dell’avvento della CHIMICA ORGANICA (22)


Università degli Studi della Campania "Luigi Vanvitelli"



Di seguito sono riportati gli studenti che, sulla base della media dei punteggi delle quattro prove sostenute, sono ammessi a sostenere la prova orale in una delle date previste dal calendario che sarà disponibile nei prossimi giorni su questo blog. Si ricorda che è necessario prenotarsi (e che è assolutamente vietato prenotarsi per più di una data). La prenotazione sarà possibile a partire dalle 00:00 del 28/12/2024 (ossia allo scattare della mezzanotte tra il 27 e il 28 dicembre) e fino a due giorni prima della data prevista per l’esame.
Gli studenti in giallo sono ammessi con riserva.
La casella relativa alla media è quella che contiene la matricola. Le altre caselle fanno riferimento a ciascuna prova sostenuta (è dunque necessario guardare la IV per avere informazioni sull’esito dell’ultima prova).
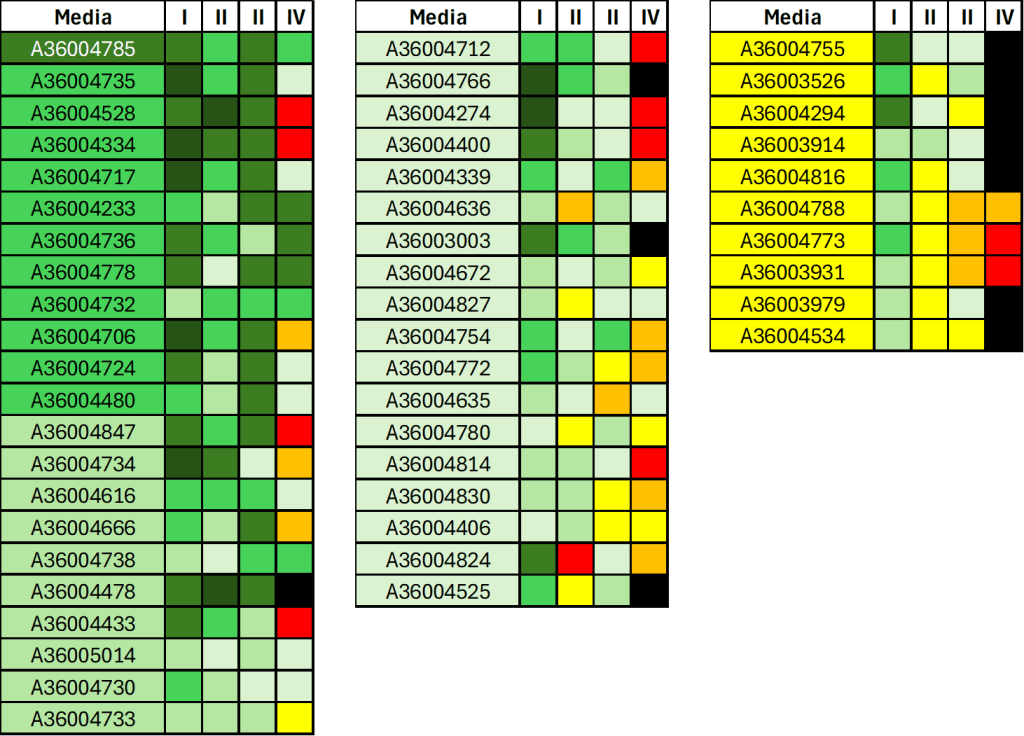
Sulla base dell’esito delle prove, gli studenti dovrebbero a questo punto essere consapevoli dei punti e degli argomenti da recuperare. In particolare, gli studenti ammessi con riserva o coloro che hanno ottenuto un punteggio più o meno disastroso in una o più prove, sono invitati a colmare tutte le loro lacune in vista dell’esame orale.
Per tutti è, infine, necessario completare l’ultima parte del programma, che non è stata oggetto delle prove scritte.
La IV prova, insieme alle correzioni, sarà resa disponibile sul blog appena possibile.
Si ricorda che le prove intercorso esonerano dallo scritto solo se si sostiene l’esame orale entro il 14 marzo
Si ricorda, inoltre, che l’intero programma sarà oggetto di discussione alla prova orale.
A gennaio sono previste esercitazioni e incontri di recupero e di riepilogo per tutti gli studenti interessati. Seguiranno ulteriori dettagli organizzativi.
ELENCO STUDENTI NON AMMESSI ALL’ESAME ORALE
Gli studenti del seguente elenco non hanno raggiunto una votazione media sufficiente per l’ammissione all’esame orale.

Gli studenti che fanno parte di questo elenco sono ammessi alla prova di recupero. Visti i risultati della III e IV prova, la prova di recupero verterà, per tutti, sugli argomenti oggetto delle 2 ultime prove intercorso. NB: potranno accedere a questa prova anche coloro che non hanno superato la III (ma la prova verterà sempre sugli argomenti di III e IV).
Ulteriori chiarimenti e informazioni, così come il form di prenotazione saranno condivisi nei prossimi giorni sul blog.
Coloro che non intendono usufrire della prova di recupero potranno sostenere la prova scritta intera in una delle date previste dal calendario.
Si ribadisce ancora una volta la disponibilità della docente a fornire ulteriori chiarimenti e si rende noto che è possibile visionare la IV prova nel corso del ricevimento. Nel corso del ricevimento, sarà possibile anche prendere visione di tutte le prove sostenute.
Dopo una breve pausa natalizia, saranno pubblicate ulteriori informazioni e materiale utile alla preparazione dell’esame orale e scritto e alle prove di recupero.

La metabolomica è una disciplina che studia l’insieme completo dei metaboliti presenti in un sistema biologico, come cellule, tessuti o organismi. Questa scienza rappresenta un’evoluzione delle scienze “omiche”, quali genomica, trascrittomica e proteomica, ed è particolarmente rilevante nell’ambito della biologia dei sistemi. Grazie all’integrazione di tecniche analitiche avanzate, come la spettrometria di massa (MS) e la risonanza magnetica nucleare (NMR), la metabolomica offre una visione globale e dettagliata del metabolismo cellulare.
Biologia dei Sistemi e il Ruolo della Metabolomica
La biologia dei sistemi è un approccio olistico che cerca di comprendere le interazioni complesse tra i vari componenti di un sistema biologico, dai livelli molecolari fino all’intero organismo. Essa si basa sull’idea che “il tutto è maggiore della somma delle sue parti”, e si avvale di modelli computazionali e matematici per descrivere tali interazioni. In questo contesto, la metabolomica fornisce informazioni chiave sullo stato funzionale delle cellule, evidenziando le attività metaboliche attuali e i cambiamenti indotti da stimoli esterni.
I metaboliti offrono una visione immediata di ciò che sta accadendo in un dato momento, completando le informazioni derivanti da DNA (ciò che è possibile), RNA (ciò che sembra stia accadendo) e proteine (ciò che lo rende possibile).
Applicazioni della Metabolomica

L’immagine illustra le principali applicazioni della metabolomica in biologia (pur non essendo esaustiva), suddivise in diversi ambiti tematici.
La metabolomica trova, dunque, applicazione in diversi ambiti della biologia e delle scienze applicate:
• Chimica delle sostanze naturali: identificazione di composti bioattivi da fonti naturali, utili per lo sviluppo di farmaci e non solo.
Il processo classico di identificazione dei prodotti naturali è stato storicamente lungo e dispendioso in termini di risorse. Un esempio pratico è lo studio condotto su Astragalus boeticus, in cui l’astragaloside è stato identificato come un candidato promettente per applicazioni farmacologiche. Questo composto ha mostrato una selettività specifica contro linee cellulari resistenti ai farmaci, rendendolo un punto di partenza per ulteriori studi preclinici. Grazie all’integrazione della metabolomica, il processo di screening è stato ottimizzato, riducendo significativamente il tempo necessario per identificare tali bioattivi. La metabolomica, combinando analisi qualitative e quantitative simultanee di un ampio numero di metaboliti, accelera significativamente questa ricerca, consentendo di individuare rapidamente candidati promettenti per applicazioni terapeutiche.
• Analisi Funzionale e Annotazione dei Metaboliti
Un’altra area di interesse è l’annotazione funzionale dei metaboliti, ossia l’assegnazione di funzioni biologiche specifiche ai composti chimici identificati. Questo approccio è cruciale per comprendere i ruoli fisiologici dei metaboliti e le loro interazioni nei sistemi biologici.
• Chemotassonomia: classificazione degli organismi basata sulle loro caratteristiche biochimiche. Questa metodologia è applicata per distinguere specie di piante attraverso l’analisi dei loro metaboliti specializzati.
• Scienze alimentari: analisi della composizione chimica degli alimenti per migliorarne qualità e sicurezza. La metabolomica consente, ad esempio, di monitorare cambiamenti nei metaboliti durante i processi di trasformazione alimentare.
• Ricerca farmacologica: scoperta di nuovi biomarcatori e terapie mirate per malattie umane. L’identificazione di composti bioattivi attraverso approcci metabolomici offre nuove opportunità per la terapia personalizzata.
• Medicina: applicazioni in questo ambito includono tutti gli aspetti che riguardano la diagnosi precoce di malattie (es. cancro), permettendo l’identificazione di specifici biomarcatori. I biomarcatori possono essere utili anche per differenziare sottotipi di malattie apparentemente simili, migliorando la precisione diagnostica. Inoltre, l’analisi dei profili metabolici può essere utilizzata per valutare l’efficacia di trattamenti medici e personalizzarli. Grazie alla metabolomica, è possibile anche adattare i trattamenti in base al profilo metabolico individuale del paziente (medicina personalizzata). È inoltre possibile, analizzando il metabolismo alterato in pazienti con specifiche patologie, comprendere i meccanismi alla base di malattie complesse.
• Risposta allo stress: studio dei meccanismi di adattamento delle piante a condizioni avverse.
• Ecologia e Studio delle Interazioni Biologiche: la metabolomica permette di approfondire lo studio delle interazioni tra organismi. In particolare:
Limiti e Sfide della Metabolomica
Nonostante i progressi, la metabolomica presenta alcune limitazioni. Ad esempio, nella stima dei flussi metabolici (fluxomics), una sfida significativa è rappresentata dalla complessità delle reti metaboliche. L’uso di isotopi marcati consente di monitorare i flussi metabolici attraverso esperimenti di labelling, ma l’interpretazione dei dati è complicata da fenomeni come i cicli futili e l’alto grado di interconnessione tra i pathway metabolici. Un esempio pratico riguarda l’analisi dei flussi in percorsi biosintetici lineari, dove l’equilibrio tra gli input e gli output può essere calcolato solo in condizioni sperimentali rigorosamente controllate.
La metabolomica è una disciplina cardine nella biologia moderna, con il potenziale di rivoluzionare la nostra comprensione dei sistemi biologici. Grazie alla sua capacità di fornire una visione globale e dettagliata del metabolismo, questa scienza continuerà a contribuire significativamente a molteplici settori della ricerca e delle applicazioni in diversi ambiti.
Utilizzando il seguente link, è possibile scaricare le slide dell’ultima lezione: https://www.dropbox.com/scl/fi/xjkdhspx3qirtqb61ikmu/11.-Metabolomica-in-biologia.pdf?rlkey=w3p94cto02mxinwi9yhmi6zez&st=b8xoyyjn&dl=0



Nelle tracce di alcuni esercizi sono indicate le pagine del libro dove è possibile trovare supporto. NB: si fa riferimento sempre all’ultima edizione del Bruice. Chi ha altri testi o edizioni vecchie del Bruice può comunque risalire alle pagine utilizzando l’indice analitico.
1) Classifica i seguenti monosaccaridi (vedi esempio a) e dire se appartengono alla serie D o alla serie L. Attribuire la configurazione assoluta a ciascun carbonio chirale .

2) I monosaccaridi a 5 e 6 termini esistono in soluzione acquosa in maniera preponderante nelle loro forme emiacetaliche cicliche. Mostrare il processo di ciclizzazione per tutti gli zuccheri dell’esercizio 1 per cui questo è possibile. Indicare il carbonio anomerico e per ciascuno disegnare sia l’anomero alfa, sia l’anomero beta.
3) Scrivere:
a) D-mannosio (il mannosio è l’epimero in 2 del glucosio)
b) L-galattosio (il galattosio è l’epimero in 4 del glucosio)
c) D-allosio (l’allosio è l’epimero in 3 del glucosio)
d) L-idosio (l’idosio è un diastereoisomero del glucosio, che ne differisce per la configurazione al C-2, C-3 e C-4)
e) il D-fruttosio (il fruttosio è un chetoso che presenta, ai carboni chirali che restano tali, le stesse configurazioni assolute del glucosio)
4) Mostrare cosa accade se mettiamo il D-mannosio (epimero in 2 del glucosio) e il D-fruttosio in ambiente basico
5) Mostrare i prodotti di riduzione con sodio boro idruro e di ossidazione col reattivo di Tollens dei monosaccaridi dell’esercizio 3.
6) Mostrare il meccanismo e i prodotti della sintesi di Kiliani-Fisher effettuata su D-treosio e su D-eritrosio. è possibile sintetizzare il D-glucosio a partire da uno dei due? Come procedereste?
7) Mostrare il meccanismo di formazione di un legame (1-4′ glicosidico) tra due unità di glucosio (facendo riferimento al meccanismo per la formazione dei glicosidi). Quale sarà il prodotto principale e perchè?
8) Dire se il disaccaride formato in 7 è uno zucchero riducente.
9) Quale delle seguenti strutture è quella del beta-L-galattopiranosio?
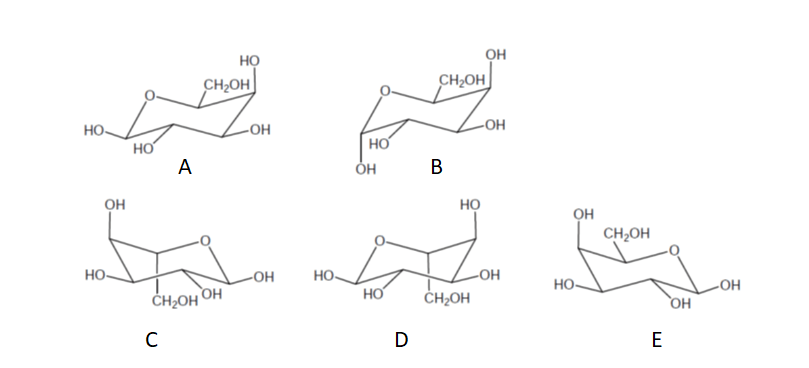
10) Dopo aver solubilizzato in acqua l’alfa e il beta D-galattopiranosio, si osserva per le due soluzioni una rotazione specifica pari a +150,7° e +52,8°, rispettivamente. Quando si effettua di nuovo la misura dopo un certo tempo, si osserva per entrambe le soluzioni una rotazione specifica pari a +80,2°. Come possiamo spiegare questa osservazione?
11) Scrivere i seguenti amminoacidi sia in proiezione di Fischer sia utilizzando le strutture a segmenti:
a) L-alanina (R=-CH3)
b) L-glutammina (R= -CH2CH2C=ONH2)
c) Acido L-aspartico (R=-CH2COOH)
d) L-cisteina (R=-CH2SH)
12) Quella riportata di seguito è la curva di titolazione dell’amminoacido alanina (R=-CH3).

a) Disegnare una curva di titolazione per l’amminoacido glicina (R=-H).
b) Di seguito è riportata la curva di titolazione per l’acido glutammico (R=-CH2COOH). Scrivere la struttura dell’amminoacido a 1) pH<2, 2) pH=3, 3) pH=7, 4) pH>10. NB: pka3 fa riferimento al pKa del gruppo ionizzabile in catena laterale; prima di affrontare questi esercizi è bene rivedere quanto studiato all’inizio del corso su acidi e basi. Consigliato anche vedere l’esercizio 51 a pagina 1026.

c) Di seguito è riportata la curva di titolazione per l’amminoacido arginina, insieme alla struttura dell’amminoacido a pH<2. Scrivere la forma zwitterionica e dire a quale valore di pH è presente. Quale sarà la struttura a pH>13?

13) Mostrare la sintesi del dipeptide alanilglicina (Ala-Gly; R =-CH3 per alanina, H per glicina).
14) Mostrare la sintesi del tripeptide glicilglicilalanina (Gly-Gly-Ala).
15) Mostrare la sintesi del tripeptide alanilglicilalanina (Ala-Gly-Ala).
16) La struttura mostrata di seguito è quella della base azotata adenina:

a) Analizzare le coppie solitarie di ciascun atomo di azoto e dire quali orbitali occupano. Per gli atomi che fanno parte del sistema ciclico, dire se le coppie solitarie contribuiscono o meno al sistema aromatico (NB: analizzarle sempre singolarmente).
b) Conoscendo la struttura di base di un nucleotide, scrivere la struttura dell’adenosina-5′-monofosfato e della 2′-deossiadenosina-5′-monofosfato (NB: in questo caso è presente deossiribosio, invece del ribosio–> “2′-deossi”).
17) Mostrare perchè è fondamentale, ai fini della stabilità del DNA, che questo contenga deossiribosio, anzichè ribosio (vedere pag. 1163, par. 26.4)
18) Quella di seguito mostrata è la struttura dell’adenosina. Facendo riferimento a questa, scrivere la struttura dell’ATP (=adenosina-5′-trifosfato) e spiegare perchè i legami fosfoanidridici sono chiamati legami ad alta energia (vedere pagg 1102-1103 del Bruice)

19) Scrivere la struttura di un trigliceride semplice in cui il glicerolo (1,2,3-propantriolo) è esterificato con un acido grasso a 18 atomi di carbonio.
20) Fornire una definizione dei lipidi
Qui potete trovare alcuni esercizi svolti (si consiglia di prendere visione di questo file solo dopo aver provato a risolvere gli esercizi in maniera autonoma)

1) Un composto è aromatico se:
1) ha una nuvola ininterrotta di elettroni π (per cui il composto deve essere ciclico, planare e ogni atomo dell’anello deve possedere un orbitale p);
2) contiene 4n+2 elettroni π (ovvero un numero dispari di coppie di elettroni π).
Un composto è antiaromatico se soddisfa il primo ma non il secondo criterio per l’aromaticità. I composti antiaromatici sono quindi ciclici, planari, possiedono una nube ininterrotta di elettroni π, ma hanno numero pari di coppie di elettroni π. I composti antiaromatici non possono riempire i loro orbitali molecolari di legame, per cui risultano molto instabili e altamente reattiviti:

Classifica i seguenti composti o ioni come aromatici, antiaromatici o non aromatici, giustificando la scelta:

2) Assegnare il nome IUPAC ai seguenti composti

3) Mostrare la sintesi delle molecole a-e dell’esercizio 2 a partire dal benzene.
4) In relazione ai composti sintetizzati nell’esercizio 3, che effetto hanno i sostituenti introdotti sulla reattività del benzene? Come orientano eventuali ulteriori sostituenti? Motivare la risposta.
5) Come sintetizzeresti il composto h dell’esercizio 3 a partire dal benzene?
Qui potete trovare alcuni esercizi svolti (si consiglia di prendere visione di questo file solo dopo aver provato a risolvere gli esercizi in maniera autonoma)

PRIMA DI SVOLGERE QUESTI ESERCIZI è NECESSARIO STUDIARE Il CAP. 17 del Bruice.
Si consiglia, inoltre, di prendere visione del materiale didattico precedentemente condiviso (in particolare, vedere il punto c). Seguendo questo link è invece possibile scaricare alcuni esercizi svolti
1) a. Individuare gli idrogeni più acidi in ciascuno dei seguenti composti. b. ordinare i seguenti composti in ordine di acidità crescente
a) 3-ossobutanoato di metile
b) acetone (=propanone)
c) acetaldeide (=etanale)
d) 2,4-pentandione
e) etanoato di metile
2) Scrivere il meccanismo e i prodotti delle seguenti reazioni

3) Proporre un metodo per la sintesi dei seguenti composti mediante condensazione aldolica (indicare le condizioni di reazioni e mostrare il meccanismo).
a) 4-epten-3-one
b) 5-metil-4-epten-3-one
c) 2-cicloesen-1-one
d) 3-metil-2-cicloesen-1-one
Suggerimento: per capire da quali composti partire, dobbiamo considerare che il carbonile presente nel prodotto di condensazione aldolica è quello del composto (o della porzione della molecola) da cui abbiamo generato lo ione enolato, mentre il carbonio beta (ora impegnato in un doppio legame C-C) era il carbonio carbonilico che ha subito l’attacco nucleofilo. Quindi, prendiamo il composto alfa,beta-insaturo e immaginiamo di saturare il doppio legame e aggiungere un gruppo -OH sul carbonio beta; immaginiamo poi di rompere il legame tra il carbonio alfa e il carbonio beta, aggiungendo un idrogeno a quello che era il carbonio alfa mentre l’ossidrile che era in beta diventerà un carbonile.
4) Proporre un metodo per la sintesi dei seguenti composti mediante condensazione di Claisen (indicare le condizioni di reazioni e mostrare il meccanismo).
a) 3-ossobutanoato di metile
b) 2,4-pentandione
c) 2-ossocicloesancarbossilato di etile
d) 1,3-cicloesandione
Suggerimento: considerare il composto ottenuto. Capire se è un beta-chetoestere o un beta-dichetone. Il primo deriverà dalla condensazione di due esteri, il secondo dalla condensazione di un estere con un chetone. Fare anche in questo caso un’analisi retrosintetica (avendo ben presente qual è il meccanismo della condensazione di Claisen).
5) Indicare i composti carbonilici di partenza che, in seguito a reazione di condensazione aldolica, forniscono il seguente composto:
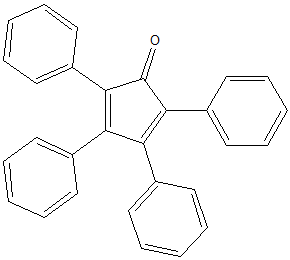
6) Le seguenti reazioni non sono utilizzabili per ottenere il prodotto mostrato in alte rese. Individuare e correggere l’errore in ciascuna reazione.

7) Come può essere preparato il seguente composto mediante reazione di Michael?
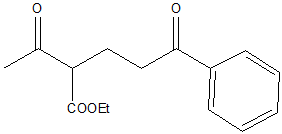
8) Proporre una strategia per sintetizzare il 2-etil-3-metil-2-pentenale utilizzando 1-butanolo come unica fonte di atomi di carbonio.
9) Proporre un meccanismo per la seguente trasformazione (potrebbero essere necessari più passaggi).

10) Proporre le condizioni e il meccanismo della seguente trasformazione
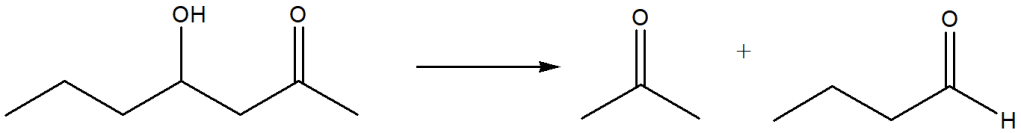
11) Sintetizzare i seguenti composti mediante condensazione aldolica o di Claisen. Indicare per ciascuno le condizioni di reazione, i reagenti, la strategia di sintesi e mostrare il meccanismo.





Sono state caricate le soluzioni dell’ultimo set di esercizi e delle due ultime challenge (per le altre si provvederà in seguito).
Per quanto riguarda gli esercizi di nomenclatura, come al solito è possibile commentare il post per ricevere le correzioni.
Per quanto riguarda i dubbi espressi nel form, qui potete consultare le risposte: https://www.dropbox.com/scl/fi/3xzduts6kqnq7sntt6ojz/Ultimi-dubbi.pdf?rlkey=dc9j5m9j2nuqzidzin9moiq28&st=lonvximr&dl=0
You must be logged in to post a comment.