Ancora esercizi su reazioni di sostituzione ed eliminazione

1) Scrivere i prodotti principali delle seguenti reazioni. Mostrare il meccanismo di reazione. Indicare la stereochimica quando opportuno. Inoltre, disegnare per ciascuna reazione il diagramma di energia libera/coordinata di reazione (corredato delle strutture degli stati di transizione e degli eventuali intermedi di reazione).
a) (S)-2-bromo-3-metilpentano + t-butossido di potassio
b) 1-bromo-1-metilcicloesano + acqua
c) 1-bromo-1-metilcicloesano + DBN
d) (2S,3R)-2-bromo-3-metilpentano + idrossido di sodio
e) (R)-2-fluorobutano + metossido di potassio
f) (clorometil)cicloesano + t-butossido di potassio
g) (1S,2R)-1-cloro-3-metilcicloesano + etossido di potassio
h) (1R,2R)-1-cloro-3-metilcicloesano + etossido di potassio
i) 3-bromocicloesene + acqua
l) 3-bromocicloesene + metossido di sodio
2) Come sintetizzeresti i seguenti composti a partire da un alogenuro alchilico e da un nucleofilo o una base? Scegliere le condizioni di reazione ottimali. Definire i reagenti e poi mostrare il meccanismo di reazione.

3) Qual è il meccanismo di reazione (SN1, SN2, E1, E2) più probabile nelle seguenti condizioni di reazione? Argomentare la scelta fatta
a) 2-bromopropano + KI in acetone;
b) 2-bromopropano + acetato di sodio in acqua;
c) 2-bromopropano + etanolo;
d) 2-bromopropano + etanolo, a caldo.
4) Quali delle seguenti affermazioni sono vere per sostituzioni nucleofile che avvengono con meccanismo SN2 e quali sono vere per sostituzioni nucleofile che avvengono con meccanismo SN1?
a) gli alogenuri terziari reagiscono più velocemente dei secondari;
b) se si usa un substrato otticamente attivo, la configurazione del prodotto è opposta a quella del prodotto di partenza;
c) la velocità della reazione dipende solo dalla concentrazione del substrato;
d) la reazione avviene in un solo stadio;
e) i carbocationi sono intermedi della reazione;
f) la velocità della reazione dipende dalla natura del gruppo uscente;
g) il 2,2-dimetil-1-cloropropano è poco reattivo.
5) Quali delle seguenti affermazioni sono tipiche di un meccanismo SN2:
a) La reazione procede con inversione di configurazione
b) L’ordine di reattività dell’alogenuro alchilico è il seguente: metile (più veloce) > 1° >2° > 3°
c) Possono avvenire riarrangiamenti
d) La velocità di reazione dipende dalla concentrazione del nucleofilo e dell’alogenuro alchilico
e) La reazione è, generalmente, più veloce in solventi polari aprotici
f) la velocità dipende dalla concentrazione del nucleofilo
g) la reazione avviene in uno stadio
h) Si forma un intermedio carbocationico
l) Si ottiene un prodotto in cui l’ibridazione del C che ha reagito è diversa da quella che aveva nel prodotto di partenza.
6) Spiegare come i seguenti cambiamenti influenzino la velocità di reazione del 2-bromo-2-metilpentano con metanolo
a) l’alogenuro alchilico è cambiato con 2-cloro-2-metilpentano
b) l’alogenuro alchilico è cambiato con 2-cloro-3-metilpentano.
7) Con riferimento agli alogenuri alchilici dell’esercizio 6, cosa cambierebbe se usassimo lo ione metossido invece del metanolo? E lo ione terz-butossido invece del metossido?
8) Srivere i prodotti principali delle seguenti reazioni (indicare anche la stereochimica dei prodotti):
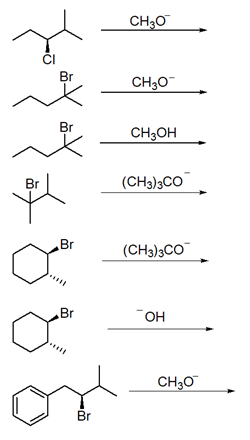
9) Ordina i seguenti composti per reattività crescente in una reazione SN1

10) Proporre un meccanismo per le seguenti trasformazioni:

SI CONSIGLIA FORTEMENTE DI SVOLGERE ANCHE GLI ESERCIZI DEL LIBRO
Queste tipologie di esercizi sono già state affrontate precedentemente, per cui non è prevista la pubblicazione di “esercizi-tipo”…Tra qualche giorno saranno pubblicate le soluzioni.
LikeLike
Esercizio 1, lettera D.. (2S,3R)-2-bromo-3-metilpentano) c’é un errore nel nome del reagente? Perché il Bromo è in posizione 2 anziché 1?
LikeLike
Perchè?
LikeLike
Prof.. Ora ho riguardato.. ero convinta fosse un ciclopentano!
LikeLike
Pingback: CdL Scienze Biologiche- Questionario su reazioni di Sostituzione ed Elimizazione degli alogenuri alchilici | Chimica Organica-DiSTABiF