esempio di un esercizio della prova intercorso

1. Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.

Si tratta di una reazione di un alchene (3-metil-2-pentene) con bromo in metanolo. Poichè questa è una reazione stereospecifica, è ESSENZIALE capire da quale isomero (E o Z) dell’alchene bisogna partire per ottenere il prodotto desiderato. Dal momento che questa reazione è anche stereoselettiva, determiniamo le configurazioni assolute dei carboni chirali, sapendo che in questo caso otterremo anche l’enantiomero.

Per capire da quale alchene dobbiamo partire, trasformiamo questa proiezione di Fisher in una rappresentazione a cavalletto, sapendo che i sostituenti sulla linea verticale si trovano lontani dall’osservatore, mentre quelli sulla linea orizzontale sono rivolti verso l’osservatore:
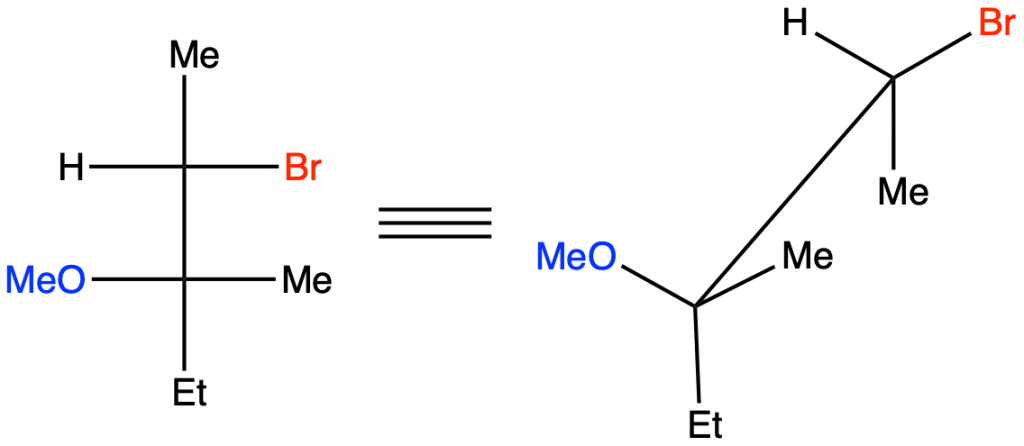
L’addizione di bromo in metanolo procede con stereochimica anti; questo significa che Br e OMe devono trovarsi da parte opposta. Ruotiamo dunque la rappresentazione a cavalletto lungo il legame C2-C3 in modo da evidenziare quanto appena detto:

L’alchene di partenza è dunque l’ (Z)-3-metil-2-pentene
MECCANISMO:
Il bromo, avvicinandosi agli elettroni pi-greco del doppio legame, si polarizza. L’attacco nucleofilo da parte dell’alchene porta alla formazione del catione bromonio e dell’anione bromuro.

Poichè la reazione viene condotta in metanolo, sarà l’alcol ad attaccare lo ione bromonio in anti rispetto al bromo; poichè la reazione è regioselettiva, il metanolo attaccherà il carbonio più sostituito (cfr. stato di transizione).
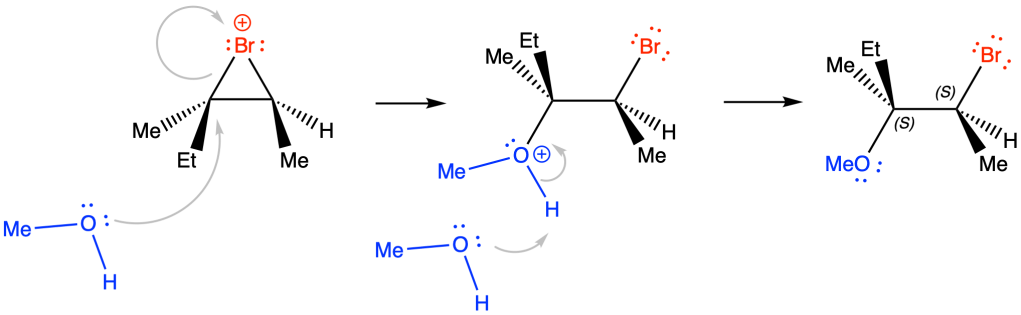
il carbonio che viene attaccato dal metanolo (conf. R) subisce inversione di configurazione con formazione del prodotto desiderato, il (2S,3S)-2-bromo-3-metil-3-metossipentano. L’attacco del bromo all’alchene dal basso, porterà alla formazione dell’enantiomero (2R,3R)-2-bromo-3-metil-3-metossipentano.
You must be logged in to post a comment.