Weekend Organic Chemistry Challenge

Regolamento:
- Vincerà la sfida chi risponderà per primo CORRETTAMENTE a tutti i seguenti quesiti.
- La risposta va inserita nei commenti al post.
- Ognuno può rispondere solo una volta (anche in presenza di più di un commento pubblicato dalla stessa persona, soltanto il primo sarà preso in considerazione).
- Il tempo massimo a disposizione sarà di 24h dalla pubblicazione del post.
- Il vincitore sarà annunciato lunedì a lezione.
Suggerimento: limitare le risposte a quanto effettivamente chiesto nelle domande!
ES. N°1
a)10 b)NEON c)1s2 2s2 2p2 d)CARBONIO
ES. N°2
a)orbitale molecolare di legame sigma b)orbitale molecolare di legame sigma c)orbitale molecolare di antilegame sigma* d)orbitale atomico p(z) e)orbitale atomico ibrido sp2 f)orbitale atomico p(y) g)orbitale molecolare di antilegame pi-greco * h)orbitale atomico ibrido sp3 i)orbitale atomico p(x)
ES. N°3
risposta: c
ES. N°4
In tutto sono presenti tre coppie di elettroni non condivisi: due per l’ossigeno, una per l’azoto.
ES. N°5
risposta: b
ES. N°6
c; b; a; d
LikeLike
1) a) 10 elettroni
b) Neon
c) 1s2 2s2 2p2
d) Carbonio
2) a) orbitale molecolare di legame sigma
b) orbitale molecolare di legame sigma
c) orbitale molecolare di antilegame sigma*
d) orbitale atomico pz
e) orbitale atomico ibrido sp2
f) orbitale atomico py
g) orbitale molecolare di antilegame pi greco*
h) orbitale atomico ibrido sp3
i) orbitale atomico px
3) risposta “c” vera
4) in tutto sono presenti 3 doppietti elettronici non condivisi. 2 per l’ossigeno e 1 per l’azoto
5) risposta “b”
6) in ordine di acidità crescente : c, b, a, d
LikeLike
1) a) 10 elettroni
b) Neon
c)1s2 2s2 2p2
d) Carbonio
2) a) orbitale molecolare di legame sigma (tra due orbitali atomici ibridi sp3)
b) orbitale molecolare sigma (tra due orbitali atomici s)
c) orbitale di antilegame sigma*
d) orbitale atomico pz
e) orbitale atomico ibrido sp2
f) orbitale atomico py
g) orbitale di antilegame pigreco*
h) orbitale atomico ibrido sp3
i) orbitale atomico px
3) c
4) sono presenti in tutto tre doppietti elettronici non condivisi, così distribuiti: sue per l’ossigeno e uno per l’azoto
5) b
6) in ordine di acidità crescente: c,b,a,d
LikeLike
1)
A-10 in totale
B- Neon
C-Carbonio
D- 1s2 2s2 2p2
2)
A- orbitale molecolare sigma di legame
B- orbitale molecolare sigma di legame
C- orbitale atomico s
D-orbitale atomico p
E- orbitale molecolare sigma
F-orbitale molecolare pi-greco
G- orbitale molecolare pi-greco di antilegame
H- orbitale ibrido
I- orbitale atomico p
3) C1 sp2;C2 sp2; N sp2;
4) 3
5) B
6) Ch4; Nh3; H2O; H2S
LikeLike
1. A) 10
B) Ne
C) 1s^2 2s^2 2p^2
D) C
2. A) orbitale molecolare di legame sigma (da orbitale atomico sp^3 + orbitale atomico sp^3)
B) orbitale molecolare di legame sigma (da orbitale atomico s + orbitale atomico s)
C) orbitale molecolare di antilegame sigma* (da orbitale atomico s + orbitale atomico s)
D) orbitale atomico pz
E) orbitali atomici ibridati sp^2
F) orbitale atomico pz
G) orbitale molecolare di antilegame sigma* (da orbitale atomico p + orbitale atomico p)
H) orbitale atomico ibrido sp^3
I) orbitale molecolare di legame sigma (da orbitale atomico sp + orbitale atomico sp)
3. c
4. 3 doppietti elettronici non condivisi
5. b
6. c, b, a, d
LikeLike
1) a. 10
b. Neon
c. 1s2 2s2 2p2
d. Carbonio
2) a. Orbitale molecolare sigma (tra s e p)
b. 1 orbitale molecolare sigma
c. antilegame sigma
d. orbitale atomico pz
e. orbitale molecolare sp2
f. orbitale atomico pz
g. antilegame pi greco
h. orbitale molecolare di antilegame sigma
i. orbitale atomico px
3) C
4) 3 doppietti elettronici non condivisi. 2 nell’O 1 in N
5) B
6) ordine crescente di acidità:
d
a
b
c
LikeLike
Mi scusi, l’ultimo ho considerato l’ordine decrescente di acidità e non crescente.
c,b,a,d
LikeLike
1) a- 10 elettroni
b- L’elemento è il Neon
c- La configurazione elettronica è 1s2 2s2 2p2
d- L’elemento è il carbonio
2) a- Orbitale molecolare di legame sigma tra due orbitali atomici ibridi sp3
b- orbitale molecolare di legame sigma tra due orbitali atomici s
c- orbitale molecolare di antilegame sigma* tra due orbitali atomici s
d- orbitale atomico p(z)
e- orbitale atomico ibrido sp2
f- orbitale atomico p(y)
g- orbitale molecolare di antilegame pigreco* tra due orbitali atomici p
h- orbitale atomico ibrido sp3
i- orbitale atomico p(x)
3) C
4) Ci sono tre doppietti elettronici non condivisi : 2 per l’ossigeno, 1 per l’azoto.
5) B
6) CH4, NH3, H20, H2S
LikeLike
1)A)8
B)NEON
C)1s2 2s2 2p2
D) CARBONIO
2) a(orbitale molecolare ibrido sigma
b) orbitale molecolare sigma
c) orbitale molecolare sigma di antilegame
d)orbitale atomico p
e ed f sono due orbitali 2p che originano orbitale molecolare pi greco
g)
h)orbitale ibrido sp3
I ) orbitale atomico p greco
3) C
4)4 doppietti
5)B
6) CH4 NH3 H2O H2S
LikeLike
1. a) 10.
b) Neon
c) 1s2 2s2 2p2
d) 4 elettroni di valenza quindi Carbonio
2. a)orbitale molecolare di legame sigma avuto dalla sovrapposizione di due orbitali atomici sp3 (in fase)
b)orbitale molecolare di legame sigma avuto dalla sovrapposizione di due orbitali atomici 1s (in fase)
c) orbitale molecolare di legame sigma
d) orbitale atomico 2pz
e) orbitale ibrido sp2
f) orbitale atomico 2py
g) orbitale molecolare di antilegame pigreco*
h) orbitale atomico ibrido sp3
i) orbitale atomico 2px
3. C
4. Sono presenti in tutto tre doppietti elettronici non condivisi in particolare : 1 per N (azoto) e 2 per O (ossigeno)
5. B
6. c,b,a,d
LikeLike
2) Aorbitale molecolare di legame sigma b)orbitale molecolare di legame sigma c orbitale molecolare di antilegame sigma* d)orbitale atomico p(z) e)orbitale atomico ibrido sp2 f)orbitale atomico p(y) g)orbitale molecolare di antilegame pi-greco * h)orbitale atomico ibrido sp3 i)orbitale atomico p(x)
1)1) a) 10 elettroni
b) Neon
c)1s2 2s2 2p2
d) Carbonio
4)3 coppie:2 sull’ossigeno e 1 sull’azoto
5)D
6) c,b,a,d
3)c
LikeLike
Aggiungo: es 1. Lettera a e b sono 8 elettroni di valenza e la configurazione elettronica è 1s2 2s2 2p6
LikeLike
1) A 10 elettroni
B) neon
C) 1s2,2s2,2p2
D) carbonio
2) a (orbitale ibrido sp3 tra due carboni)
b orbitale molecolare
c orbitale atomico tipo s
d orbitale atomico tipo p
e orbitale ibrido tipo p
f orbitale atomico f tipo p
g orbitale molecolare tipo p
h orbitale molecolare
i orbitale ibrido
3) C
4) 2 dell’ossigeno e 1 dell’azoto
5) a
6) CH4, NH3, H2O, H2S
LikeLike
1)
A. In totale ci sarebbero 10 elettroni.
B. Un atomo che possiede 10 elettroni in totale, quindi 8 elettroni nel secondo livello energetico più esterno, è il Neon.
C. Se fossero presenti solo 2 elettroni negli orbitali 2p, la configurazione dell’atomo sarebbe 1s²2s²2p².
D. L’atomo che corrisponde a questa configurazione è il Carbonio.
2)
A. Si tratta di un orbitale molecolare di legame sigma, ottenuto dalla sovrapposizione assiale di due orbitali atomici ibridi sp³.
B. Si tratta di un orbitale molecolare di legame sigma, ottenuto dalla sovrapposizione in fase di due orbitali atomici s.
C. Si tratta di un orbitale molecolare di antilegame sigma*, ottenuto dalla sovrapposizione fuori fase di due orbitali atomici s.
D. Si tratta di un orbitale atomico pz.
E. È un orbitale ibrido sp², dato dalla combinazione di un orbitale atomico s e due orbitali atomici p.
F. È un orbitale atomico pz.
G. Si tratta di un orbitale molecolare di antilegame pi greco*, ottenuto dalla sovrapposizione laterale fuori fase di due orbitali atomici p.
H. È un orbitale atomico ibrido sp³, dato dalla combinazione si un orbitale s e tre orbitali p. (25% carattere s e 75% carattere p).
I. È un orbitale atomico px.
3)
risposta: C (C1: sp²; C2: sp²; N: sp²).
4)
In tutta la molecola sono presenti in totale 3 doppietti elettronici: due coppie sull’ossigeno e una coppia sull’azoto.
5)
Risposta: B. Una coppia di elettroni sull’azoto terminale instaura il triplo legame con l’azoto adiacente. Di conseguenza il doppio legame tra azoto-carbonio si spezza e il doppietto elettronico di legame ai dispongono sul Carbonio come coppia solitaria.
6)
Ordine: c, b, a, d.
L’acidità di un composto aumenta all’aumentare dell’elettronegatività, considerando anche l’aumento di dimensioni dell’atomo.
LikeLike
ESERCIZIO 1
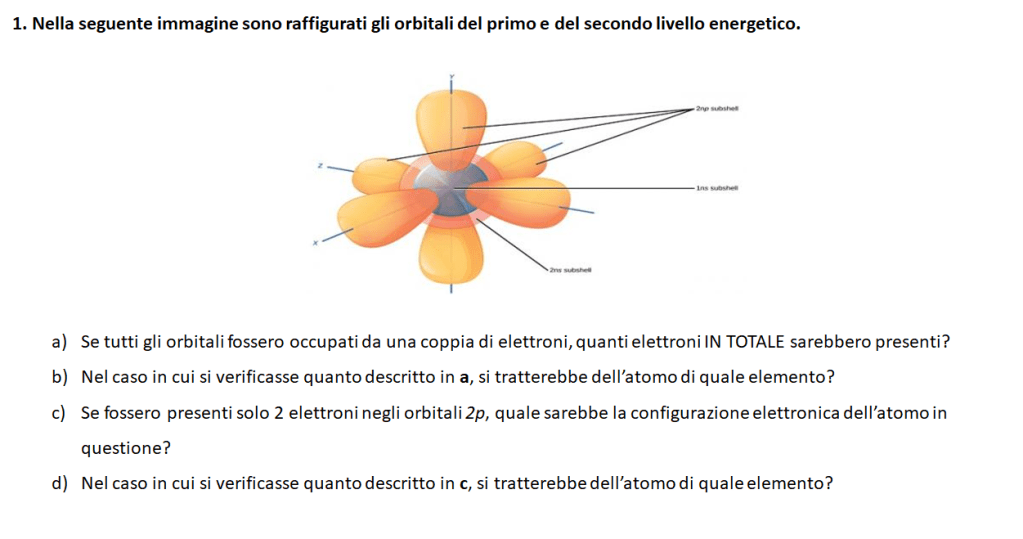
A) Se tutti gli orbitali fossero occupati da una coppia di elettroni, il numero di elettroni totale sarebbe pari a 10 (2 elettroni nell’orbitale 1s, 2 elettroni nell’orbitale 2s e 6 elettroni nei 3 orbitali p del 2° livello).
B) L’atomo che possiede 10 elettroni in totale e dunque 8 elettroni nel livello energetico di valenza, è l’atomo del gas nobile NEON.
C) Se fossero presenti solo 2 elettroni negli orbitali 2p, la configurazione elettronica dell’atomo sarebbe: 1s2 2s2 2p2.
D) Nel caso in cui l’atomo avesse la configurazione suddetta al punto C, avrebbe 4 elettroni di valenza (2° livello = livello energetico di valenza), dunque si tratta dell’atomo di CARBONIO.
ESERCIZIO 2
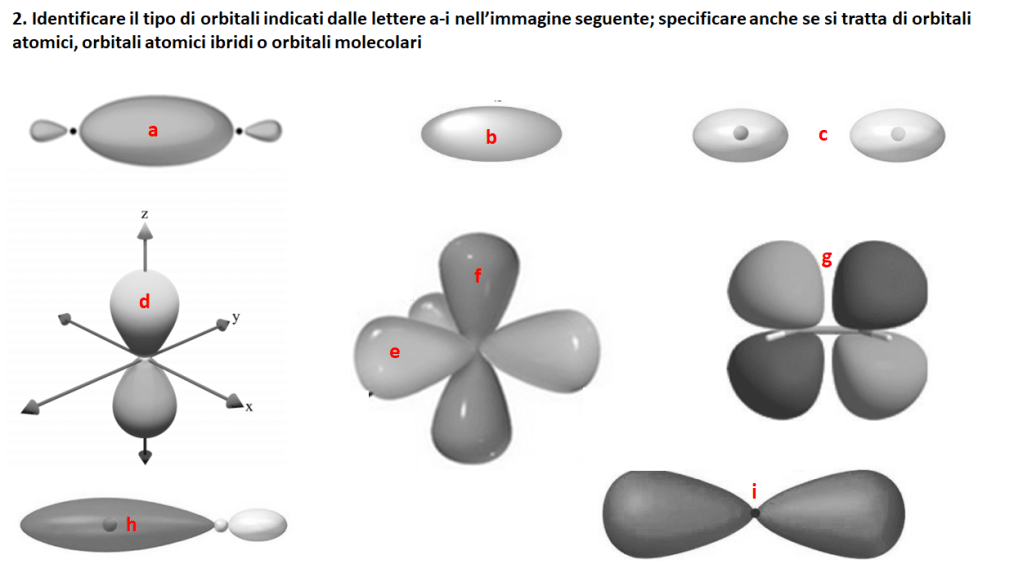
A) Orbitale molecolare di legame sigma, dato dalla sovrapposizione di 2 orbitali atomici ibridi sp3, ottenuti dall’ibridazione di un orbitale s e 3 orbitali p.
B) Orbitale molecolare di legame sigma, dato dalla sovrapposizione di 2 orbitali atomici s.
C) Orbitale molecolare di anti-legame sigma* ottenuto dalla sovrapposizione non in fase di 2 orbitali atomici s.
D) Orbitale atomico pz (composto da un lobo maggiore e un lobo minore con differenti fasi.
E) Orbitale atomico ibrido sp2, ottenuto dalla combinazione di un orbitale s e 2 orbitali p.
F) Orbitale atomico pz.
G) Orbitale molecolare di antilegame pi-greco* ottenuto dalla sovrapposizione non in fase di 2 orbitali atomici p.
H) Orbitale atomico ibrido sp3, ottenuto dalla combinazione di un orditale atomico s e 3 orbitali atomici p. Dunque questo avrà il 25% di carattere s e il 75% di carattere p.
I) Orbitale atomico px.
ESERCIZIO 3
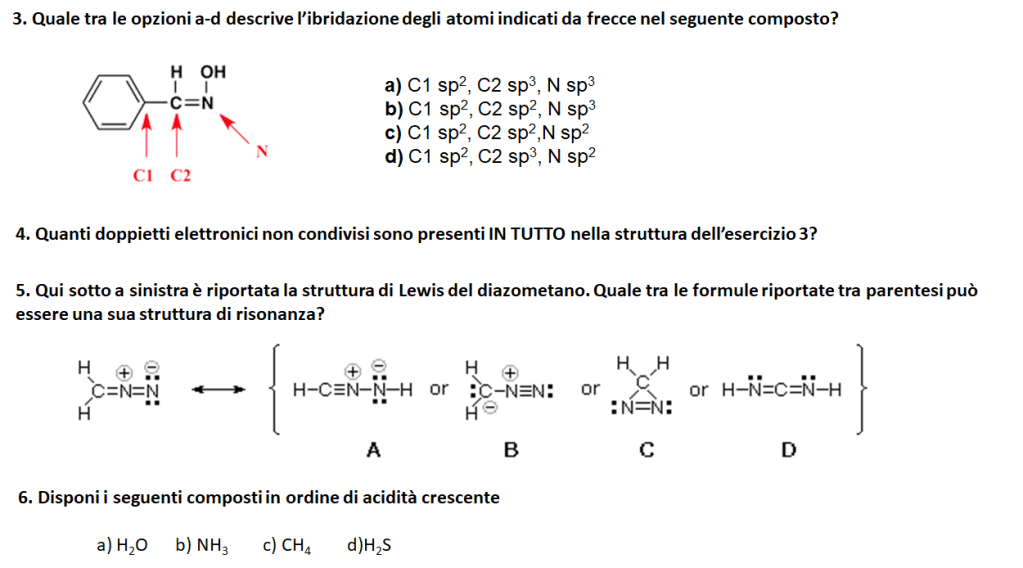
C) C1 sp2, C2 sp2, N sp2.
ESERCIZIO 4
Nella struttura del composto dell’esercizio 3 sono presenti 3 doppietti elettronici non condivisi, 2 coppie solitarie sull’atomo di ossigeno e una coppia solitaria sull’atomo di azoto.
ESERCIZIO 5
La formula B rappresenta la struttura di risonanza del composto. Una coppia di elettroni sull’atomo di azoto terminale forma il legame con l’altro atomo di azoto, di conseguenza il legame tra azoto e carbonio (N-C) si rompe e gli elettroni di legame passano sull’atomo di carbonio come coppia solitaria. Il carbonio a questo punto ha carica formale – poiché possiede un numero di elettroni pari a 5 rispetto al numero di elettroni di valenza dell’atomo neutro.
ESERCIZIO 6
C B A D (acidità aumenta con l’aumentare dell’elettronegatività e delle dimensioni atomiche)
LikeLike
Esercizio 1
a) 10 elettroni
b) Neon
c)1s2 2s2 2p2
d)Carbonio
Esercizio 2
a)orbitale molecolare di legame sigma tra 2 orbitali atomici sp3
b)orbitale molecolare di legame sigma tra 2 orbitali atomici s
c)orbitale molecolare di antilegame sigma* tra 2 orbitali atomici s
d)orbitale atomico pz
e)orbitale atomico ibrido sp2
f)orbitale atomico py
g)orbitale molecolare di antilegame pigreco*
h)orbitale atomico ibrido sp3
i)orbitale atomico px
Esercizio 3
Risposta C
Esercizio 4
Ci sono 3 doppietti elettronici non condivisi: 2 per l’ossigeno e 1 per l’azoto
Esercizio 5
Risposta b
Esercizio 6
c, b, a, d
LikeLike
ES 1
a. 10; b. NEON; c. 1s2 2s2 2p2; d. CARBONIO
ES 2
a. Orbitale molecolare di legame sigma formato dalla sovrapposizione assiale di due orbitali atomici ibridati sp3 in fase
b. Orbitale molecolare di legame sigma formato dalla sovrapposizione di due orbitali atomici s
c. Orbitale molecolare antilegame sigma* formato dalla combinazione distruttiva di due orbitali s
d. Orbitale atomico p(z)
e. Orbitale ibrido sp2
f. Orbitale p(y)
g. Orbitale antilegame π*
h. orbitale atomico ibrido sp3
i. Orbitale atomico p(x)
ES 3: C
ES 4: sono presenti tre coppie di elettroni non condivise, due coppie per l’ossigeno e una coppia per l’azoto
ES 5: B
ES 6: c-b-a-d
LikeLike
1) a=10
b= neon
c= 1s2 2s2 2p2
d= carbonio
2)a= orbitale molecolare sigma di legame
b= orbitale molecolare sigma di legame
c= orbiatale molecolare sigma di antilegame
d= orbitale atomico 2p
e- f= orbitali atomici ibridi 2p
g= orbitale molecolare pi greco di antilegame
h= orbitale molecolare
i= orbitali sp ibridi
h= orbitale atomico sp3
3) risposta C
4) doppietti elettronici 3 : 2 su ossigeno e 1 su N
5) B
6)ks2 h2o nh3 ch4
LikeLike
1 a)10 b)neon c)1s2 2s2 2p2 d)carbonio
2 a) orbitale molecolare di legame sigma dato da 2 sp3 b)orbitale molecolare di legame sigma dato da 2 orbitali 1s c)2 orbitali atomici 1s d)orbitale atomico 2p(z) e)orbitale ibrido sp2 f)orbitale 2p(z) non ibridato g)orbitale molecolare di antilegame pigreco* h)orbitale ibrido sp3 i)orbitale atomico p(x)
3 C
4 3
5 B
6 c,b,a,d
LikeLike
ES n°1
A) 10 elettroni
B) Neon
C) 4 elettroni
D) Carbonio
ES n° 2
A) Orbitale molecolare di legame sigma
B) Orbitale molecolare sigma
C) Orbitale molecolare di antilegame sigma
D) Orbitale atomico Pz
E) Orbitale atomico sp2
F) Orbitale atomico Pz
G) Orbitale molecolare di antilegame pi-greco
H) Orbitale ibrido sp3
I) Orbitale atomico Px
ES n°3 e 4
Risposta C: il C1 è ibridato sp2, il C2 sp2 e N sp2
3 doppietti elettronici non sono condivisi: uno posto sull’azoto, due invece sull’ossigeno
ES n°5
La struttura di risonanza corretta è quella raffigurata dalla risposta B
Es n°6
CH4>NH3>H2O>H2S
LikeLike