AULE PER VISIONE COMPITO
Gli studenti prenotati per visionare il compito dovranno presentarsi all’oraio prefissato in a
AULA SB (martedì/mercoledì/giovedì)
AULA GAIA (Venerdì)
Università degli Studi della Campania "Luigi Vanvitelli"
Gli studenti prenotati per visionare il compito dovranno presentarsi all’oraio prefissato in a
AULA SB (martedì/mercoledì/giovedì)
AULA GAIA (Venerdì)

Regolamento:

Qui potete scaricare materiale relativo alla prochiralità

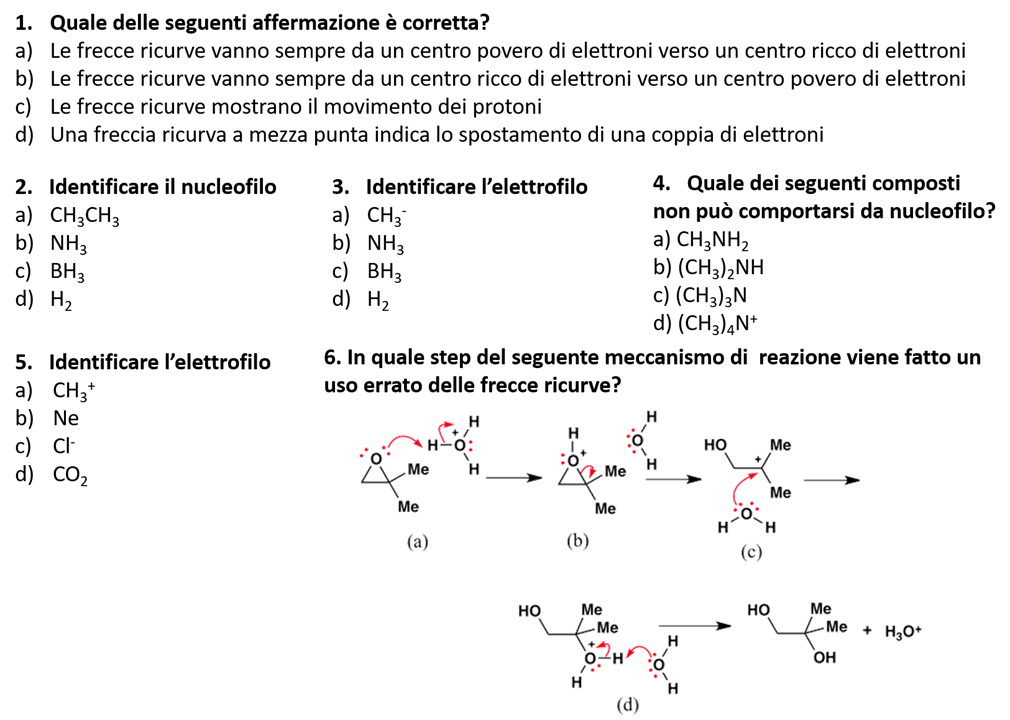
7) Dire quali delle seguenti specie chimiche tenderanno a reagire come nucleofili e quali come elettrofili

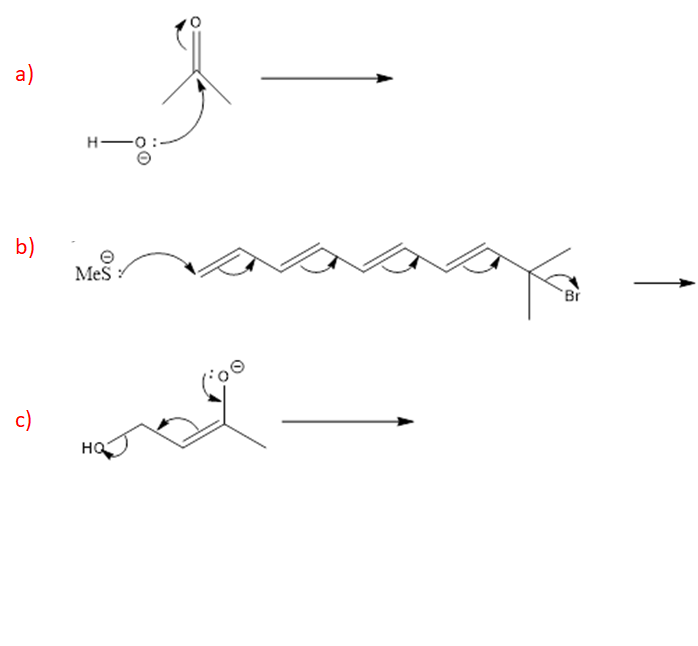
8) Sulla base del movimento degli elettroni mostrato dalle frecce ricurve nelle seguenti reazioni, disegnare i prodotti
9) Queste due reazioni formano i prodotti mostrati, ma non attraverso i meccanismi disegnati! Per ciascun meccanismo, spiegare perchè è errato e disegnarne uno corretto


1) Assegnare il nome IUPAC comprensivo di stereochimica ai seguenti composti.
NB: per cicli di piccole dimensioni non è necessario dire se il doppio legame ha geometria E o Z, dato che esiste una sola possibile geometria per il doppio legame (la geometria opposta genererebbe troppa tensione angolare). Per cicli con 8 o più atomi di carbonio dobbiamo invece indicare la geometria del doppio legame.
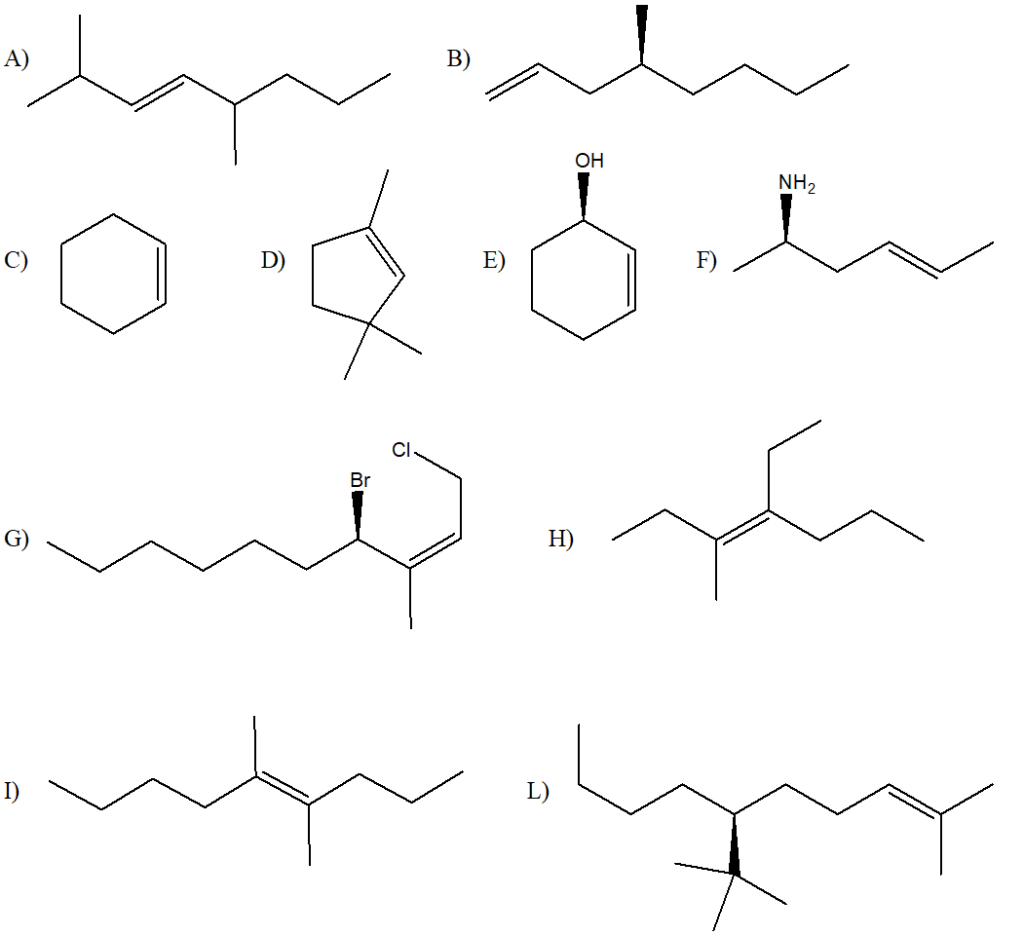
2) Scrivere le strutture corrispondenti ai seguenti nomi sistematici:
a) (2E)-2-esene
b) (3Z)-3-metil-3-esene
c) 4-isobutilcicloesene
d) (3E)-4-(clorometil)-3-etil-3-eptene
e) 3-sec-butil-1-etilciclopentene
3) Esistono quattordici alcheni di formula C6H12. Disegnateli e denominateli

VISIONE PROVA INTERCORSO
Gli studenti che hanno sostenuto la prova intercorso potranno visionarla:
1) prenotando il ricevimento utilizzando il solito link
2) prenotando il ricevimento dedicato solo alla visione della prova intercorso, utilizzando il seguente link: VISIONE PROVA
DIFFICOLTà PROVA INTERCORSO
Coloro che hanno avuto, nell’affrontare la seconda prova, difficoltà non ascrivibili alla mancanza/carenza di studio ed esercizio, possono utilizzare il seguente form per esprimerle: DIFFICOLTà II PROVA. In alternativa, potranno prenotare un colloquio (–>ricevimento) con la docente.
PROVE DI RECUPERO
Non sono previste prove di recupero durante il corso, ma tutti coloro che non hanno superato la prima o la seconda prova e intendono dare l’esame a fine corso sono invitati a continuare a seguire con costanza. A breve saranno organizzati degli incontri di recupero e a fine corso riceverete informazioni su modalità di esame a voi dedicate.
ESERCITAZIONI AGGIUNTIVE SU RAPPRESENTAZIONI DELLE MOLECOLE
Gli studenti interessati a fare delle esercitazioni aggiuntive sulle rappresentazioni delle molecole potranno prenotarsi utilizzando il seguente link: https://forms.office.com/Pages/ResponsePage.aspx?id=73pUj9cUykmk1FGmxcuSwXTRdKT1SyhLnKfYH_H9vfJUQlBNOVJKTTRMRFFWMU44NFBPWDU2UkJBSiQlQCNjPTEu. Il form si chiuderà domani, 6 novembre, alle 21:00.

No, non si tratta di un errore nel titolo.
Di seguito sono riportati alcuni degli errori gravissimi fatti nella prova.
1) Partiamo da quello meno grave, in quanto può essere risolto esercitandosi di più: problemi con l’attribuzione della configurazione assoluta e nelle interconversioni da una rappresentazione all’altra. Si raccomanda di prendere visione anche del materiale didattico presente qui sul blog.
2) L’analisi conformazionale a volte è fatta in maniera confusa e caotica: nello scrivere le varie conformazioni è importante non ruotare mai contemporaneamente entrambi i carboni di una proiezione di Newman. Sceglietene uno e ruotate sempre e solo quello e sempre nella stessa direzione.
3) NON ESISTONO legami equatoriali e assiali in una proiezione di Newman di un composto a catena lineare.
4) Il composto mostrato a sinistra è correttamente rappresentato dalle due sedie a destra. Queste due conformazioni si interconvertono l’una nell’altra (passando attraverso le altre conformazioni del cicloesano). Ne consegue che se devo confrontare una struttura a segmenti con una sedia NON potrò MAI dire che le due strutture sono isomeri conformazionali (in quanto quella a sinistra è rappresentata da entrambe le sedie a destra)
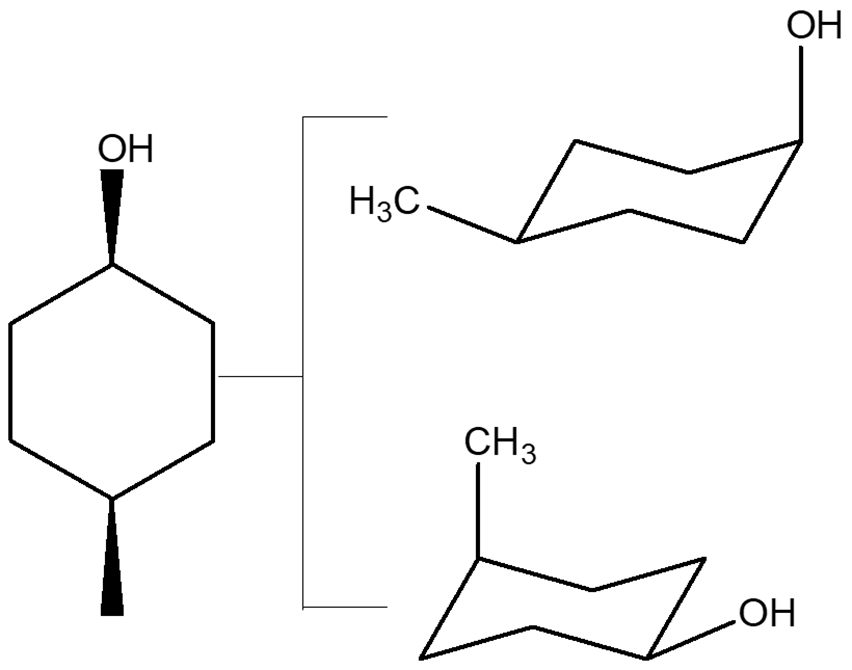
5) Il composto in alto non è chirale, per cui, se lo confronto con qualsiasi altro cicloesano sostituito, questi non potranno essere tra loro isomeri ottici.
6) S–>R e viceversa. S NON DIVENTA MAI R (e viceversa) ammenochè non rompiamo dei legami e scambiamo dei sostituenti. Il sistema di Cahn-Ingold-Prelog (CIP) ci impone di osservare la molecola in modo da avere il sostituente a priorità minore lontano dall’osservatore. Se questo è rivolto verso l’osservatore, è chiaro che sto guardando la molecola dal lato diametralmente opposto a quello prescritto da CIP, per cui rotazione oraria corrisponderà in questo caso a configurazione assoluta S e antioraria a R
7) Collegato al punto 6, se il sostitutente a priorità minore è sul piano NON POSSO attribuire la configurazione assoluta. E’ NECESSARIO effettuare una rotazione. Data la difficoltà di immaginare questa rotazione, il modo più semplice per attribuire la configurazione assoluta a questo carbonio è: I) fare uno scambio (in questo caso, sì che cambia la configurazione dato che ottengo l’enantiomero del composto iniziale) portando il sostituente a priorità minore lontano dall’osservatore e II) attribuire la configurazione all’enantiomero del composto di partenza. Nota questa, è nota anche quella del composto iniziale.
8) Nomenclatura: a) è essenziale usare correttamente virgole, trattini, parentesi, ecc. b) non è possibile dimenticare le regole di nomenclatura (e se questo succede, è il caso di rivederle) ed andare in confusione quando le rappresentazioni strutturali cambiano leggermente. Vediamo due esempi presenti nella prova:
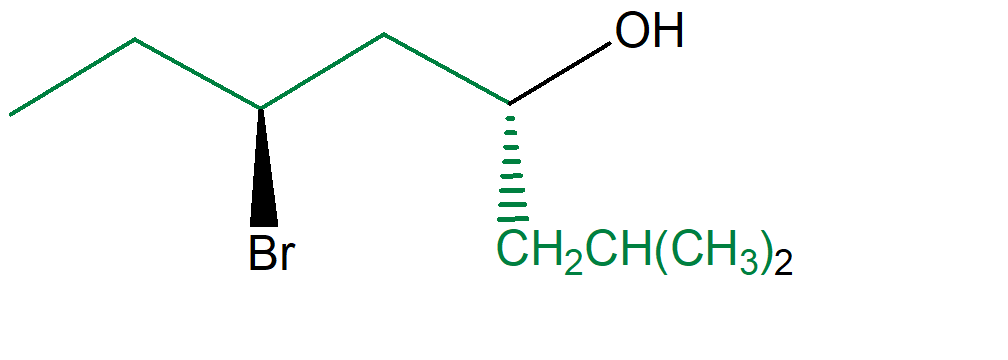
La catena principale è indicata in verde: quella continua più lunga contenente il carbonio che lega il gruppo funzionale. Il carbonio 1 sarà quello presente ad una estremità, e in particolare a quella che mi permette di attribuire il numero più basso possibile al carbonio che lega il gruppo funzionale. Questo composto si chiamerà:
(4R,6S)-6-bromo-2-metil-4-ottanolo.
A seguire un altro esempio (la catena principale è anche qui indicata in verde):
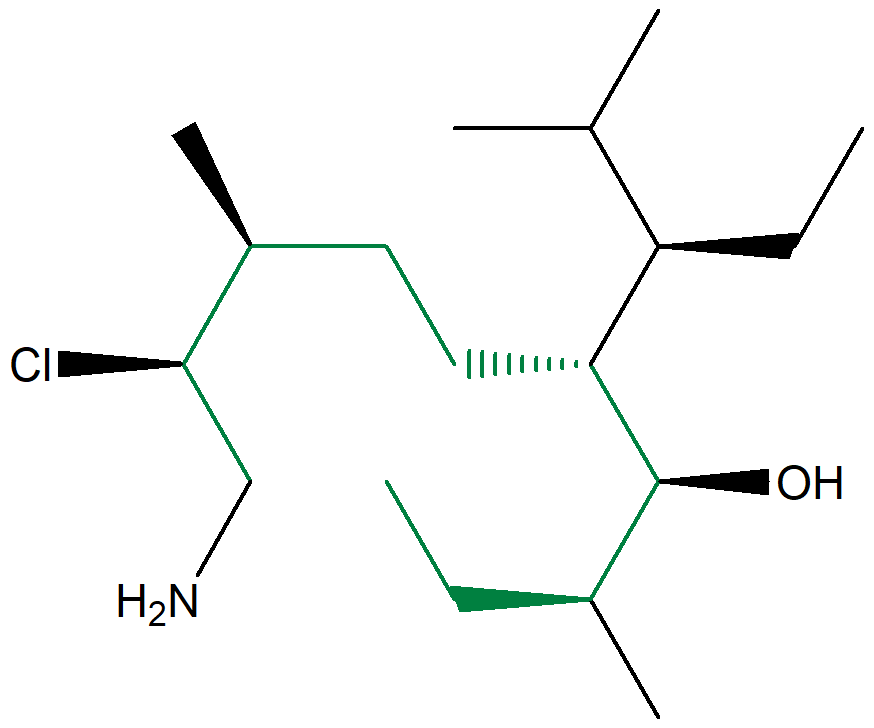
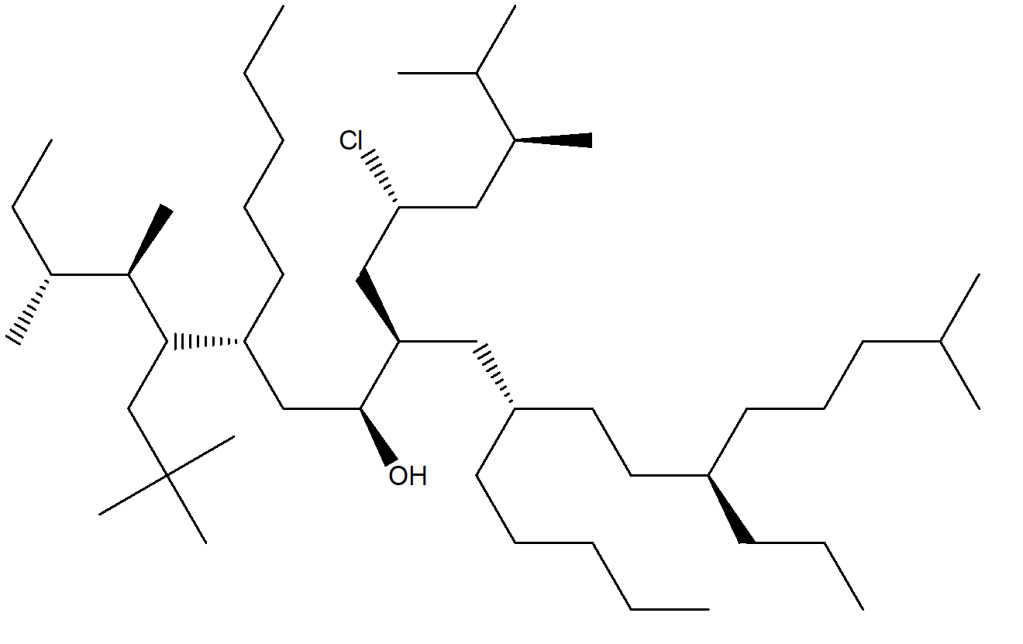
(3S,4S,5R,8S,9S)-10-ammino-9-cloro-5-[(1R)-1-etil-2-metilpropil]-3,8-dimetil-4-decanolo

Per poter convertire agevolmente una rappresentazione strutturale in un’altra è essenziale aver compreso a fondo ogni singola rappresentazione. Per questo, in caso di dubbi, è necessario far riferimento al libro e alle note precedentemente condivise (incluse quelle presenti a questo link).

Un punto importante da precisare è che queste rappresentazioni guardano il legame cabonio-carbonio da diverse prospettive, ed è essenziale sapere da quale angolazione è osservata la molecola. Un’altra cosa da aver chiara, è che è possibile scrivere più rappresentazioni di uno stesso composto (anche dello stesso tipo), semplicemente cambiando il punto di osservazione. Scegliere la prospettiva ottimale che ci permette di fare le operazioni di conversione in maniera agevole è sicuramente vantaggioso, ma potrebbe essere utile anche provare a utilizzare anche punti di osservazione diversi.
Qui vedremo qualche altro esempio. Immaginiamo di voler rappresentare, in varie forme, il (2S,3R)-3-bromobutan-2-olo. Qui rappresentato con una struttura a segmenti:

Ricordiamo che i legami non esplicitati sui carboni chirali sono legami che il carbonio fa con l’idrogeno, per cui:
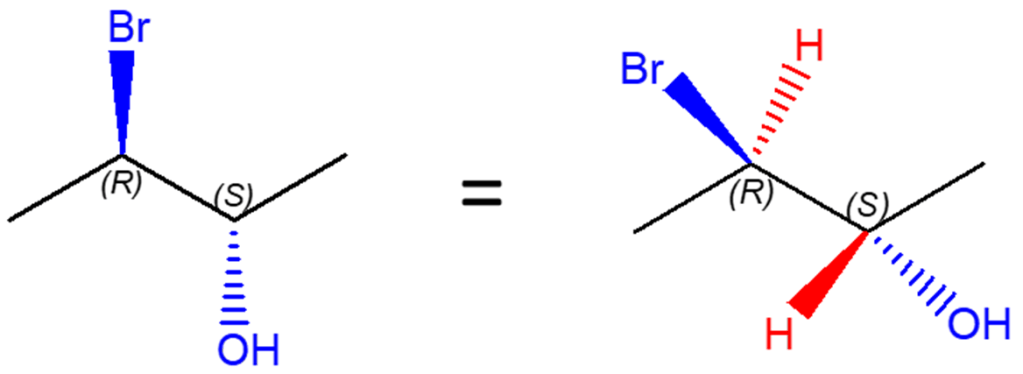
La struttura a destra somiglia già a quella che è una formula prospettica:

Nelle varie conversioni che seguiranno, i legami con gli idrogeni saranno sempre riportati in rosso. Fate attenzione alla lora posizione relativa. Inoltre, osservate bene sempre quale dei due carboni chirali è il 2 (quello che lega -OH) e qual è il 3 (quello che lega -Br). Notate inoltre come la configurazione assoluta dei carboni chirali non cambia MAI.
Un altro punto da chiarire è che è possibile ottenere rappresentazioni dello stesso composto da diverse prospettive.
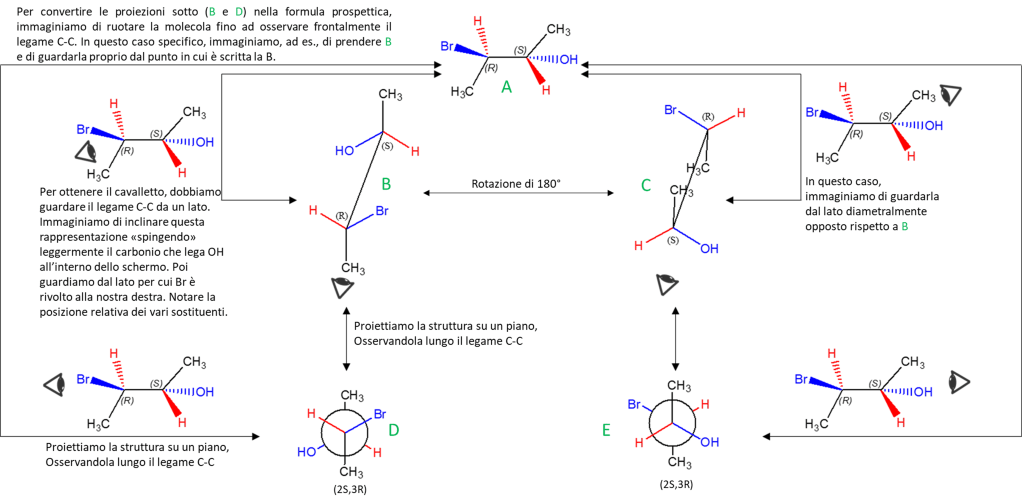
Sappiamo già come ottenere le conformazioni eclissate nelle proiezioni di Newman e a cavalletto, ma è possibile eclissare i legami anche nella formula prospettica:

A questo punto, possiamo fare le stesse operazioni viste prima su questa formula eclissata. In questo caso, possiamo scrivere anche la proiezione di Fischer (NB: per farlo, è ovviamente anche possibile eclissare le strutture a cavalletto o le proiezioni di Newman precedentemente scritte).

Il punto di osservazione ottimale per convertire le strutture a cavalletto e le proiezioni di Newman a Fischer è già stato chiarito nel post precedente e a lezione, ma vediamo cosa succede se eclisso le strutture, dirigendo la “V” verso il basso.
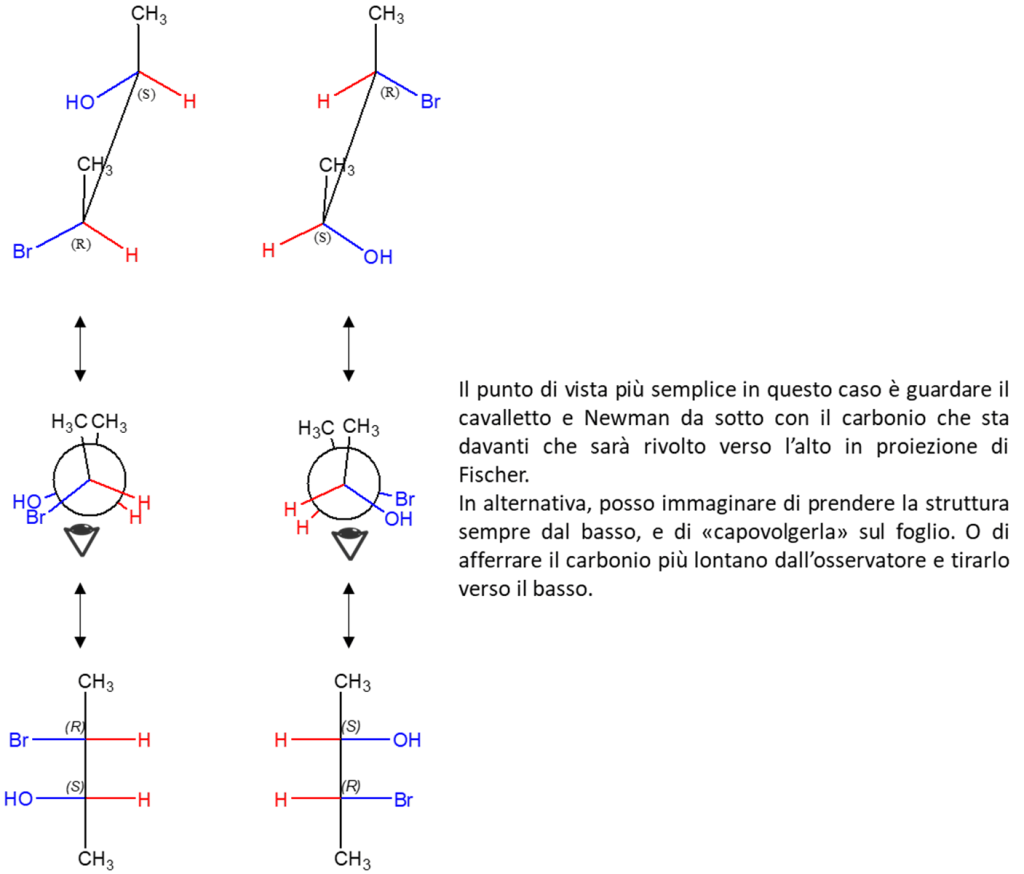
I punti di osservazioni mostrati qui sono solo alcuni di quelli possibili. Nella figura in basso si mostra, ad es., come è possibile osservare una stessa struttura a cavalletto, ottenendo due diverse formule prospettiche (che ovviamente sono equivalenti in quanto rappresentano sempre lo stesso composto). Da ogni formula sfalsata, si ottiene poi anche quella eclissata.
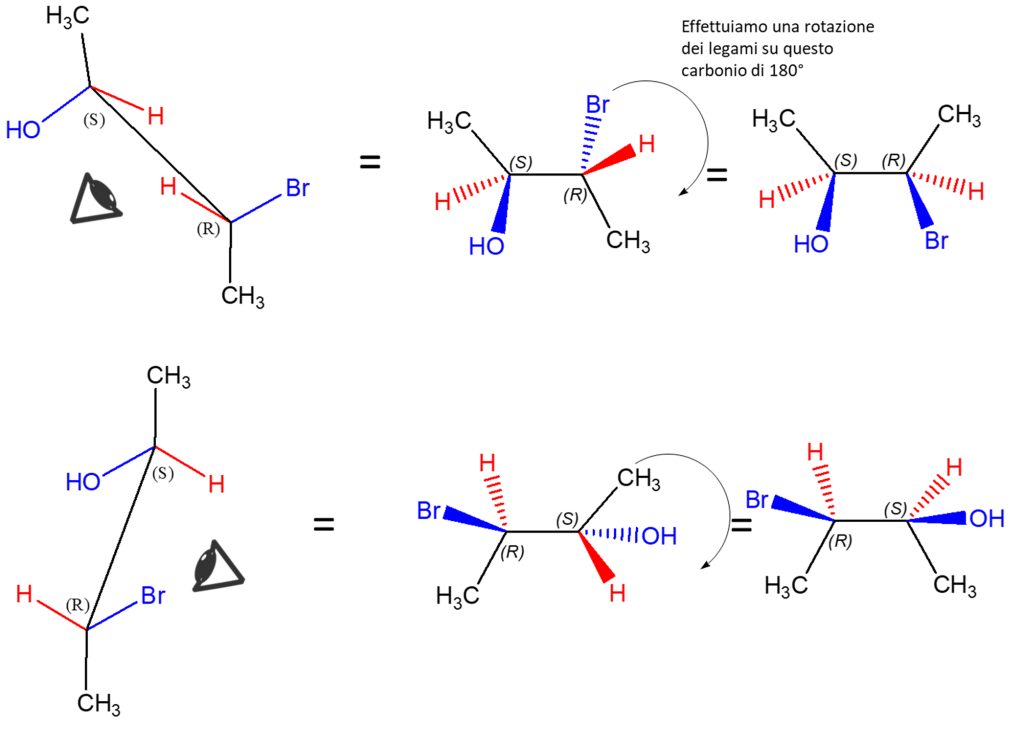
Nell’immagine seguente, un altro esempio. Una proiezione di Newman osservata da tutti i possibili punti di vista per convertirla in proiezione di Fischer. Nell’osservarla e nel confrontare le proiezioni di Fischer, fate attenzione a confrontare sempre il carbonio 2 su una proiezione con lo stesso carbonio sull’altra proiezione, non essendo sempre il carbonio 2 quello scritto più in alto (le proiezioni di Fischer a destra sono ruotate di 180° nel piano del foglio rispetto a quelle a destra).

O ancora, di seguito trovate tre dei possibili punti di osservazione di una formula prospettica (ma questi non sono tutti: è possibile osservarla anche da altri punti di vista, semplicemente ruotandola, o ad esempio guardandola dalle stesse angolazioni, ma “a testa in giù”… il che equivale ad una rotazione di 180° sul piano del foglio per la proiezione di Fischer). Il colore della proiezione di Fischer corrisponde al punto di osservazione indicato da una freccia dello stesso colore.

Esiste un solo modo per prendere familiarità con queste interconversioni: esercitarsi. Basta scegliere un composto e provare a interconvertirne le varie rappresentazioni, usando anche più punti di osservazione. All’inizio potrebbe essere utile usare i modellini a supporto dell’immaginazione… E per controllare di non aver fatto errori: attribuire il nome IUPAC, comprensivo di stereochimica. Se due strutture hanno lo stesso nome, inclusa la notazione della configurazione assoluta, sono rappresentazioni dello stesso composto.

Di seguito sono riportati i risultati della seconda prova intercorso.
La casella relativa alla media delle prime due prove è quella che contiene la matricola. La media determina l’ammissione alla prova successiva. Le altre caselle fanno riferimento a ciascuna prova sostenuta.
In particolare, si prega di prendere visione dei risultati della II prova.
Gli studenti identificati con il colore verde (casella della media) sono ammessi a sostenere la seconda prova intercorso (ovviamente, l’ammissione è subordinata alla frequenza alle lezioni, secondo quanto già chiarito precedentemente).
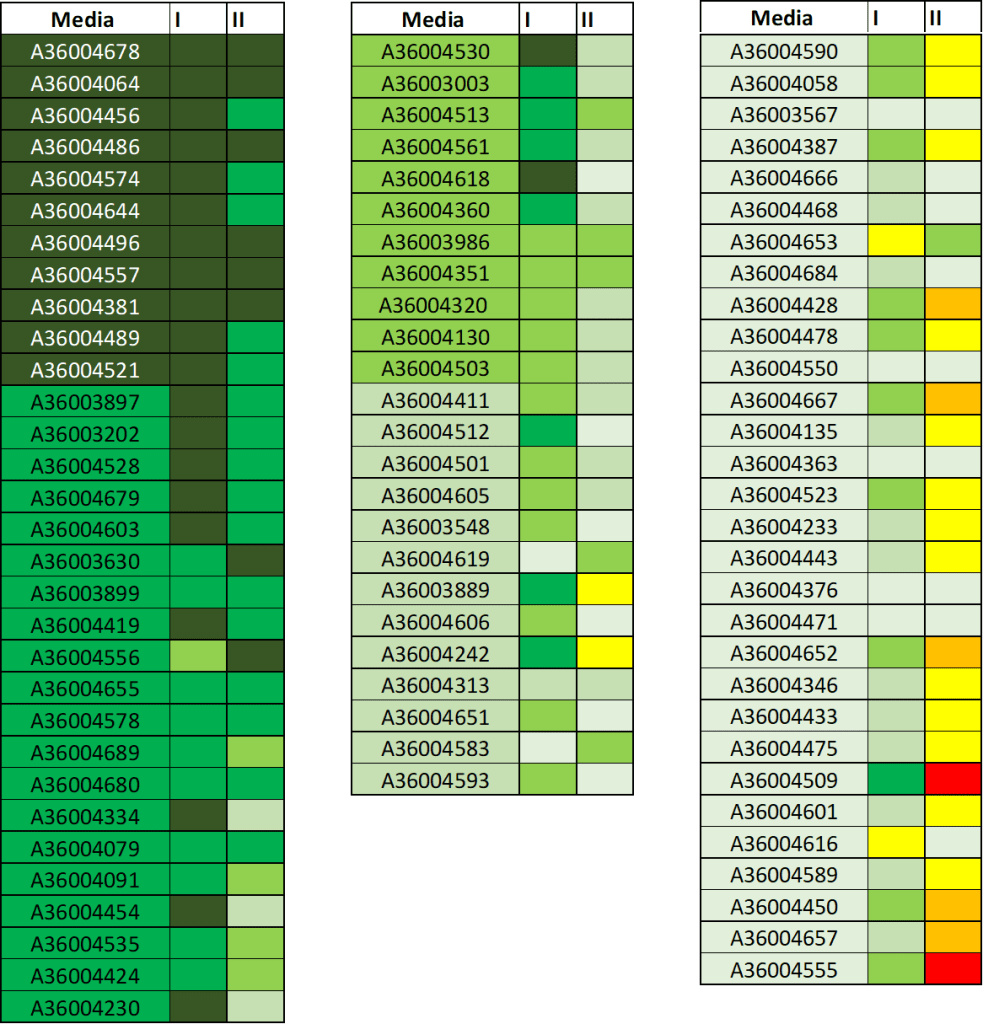
NB: I BONUS ottenuti dalla vittoria della Weekend Organic Chemistry Challenge (e delle sfide a sorpresa) sono già stati aggiunti nel conteggio del punteggio finale.
Gli studenti identificati dai colori giallo e arancione, di seguito riportati, sono ammessi con riserva alla terza prova intercorso
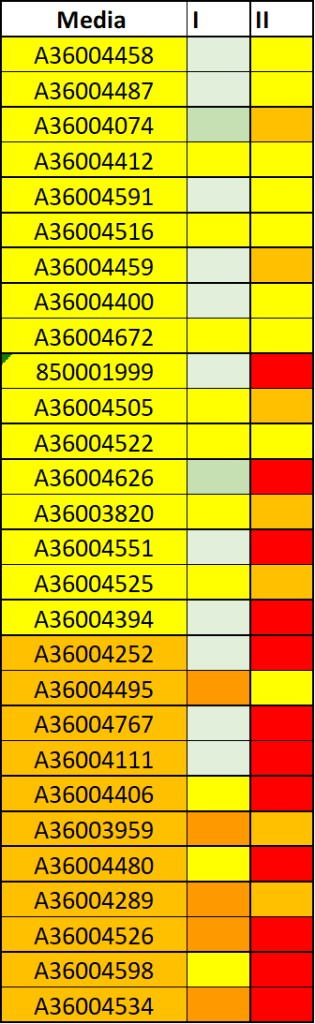
Gli studenti che fanno parte di questo gruppo sono VIVAMENTE INCORAGGIATI a rivedere gli argomenti oggetto delle prime due prove al fine di colmare lacune e chiarire dubbi. Allo stesso modo, sono incoraggiati ad agire al più presto in questa direzione coloro che, pur essendo stati ammessi alla terza prova con una media sufficiente, hanno dimostrato una scarsa conoscenza degli argomenti della seconda prova (vedere caselle gialle, arancioni e rosse del gruppo precedente). Si ricorda che è possibile chiedere il supporto della docente. A lezione saranno illlustrate eventuali misure aggiuntive per questi studenti.
Di seguito sono riportati gli studenti NON AMMESSI a sostenere la Terza Prova Intercorso
Si ricorda che il nero indica una insufficienza gravissima (voto minore di 6…e si ricorda che i voti sono espressi in trentesimi).

Seguiranno informazioni sulle modalità in cui sarà possibile prendere visione della prova.

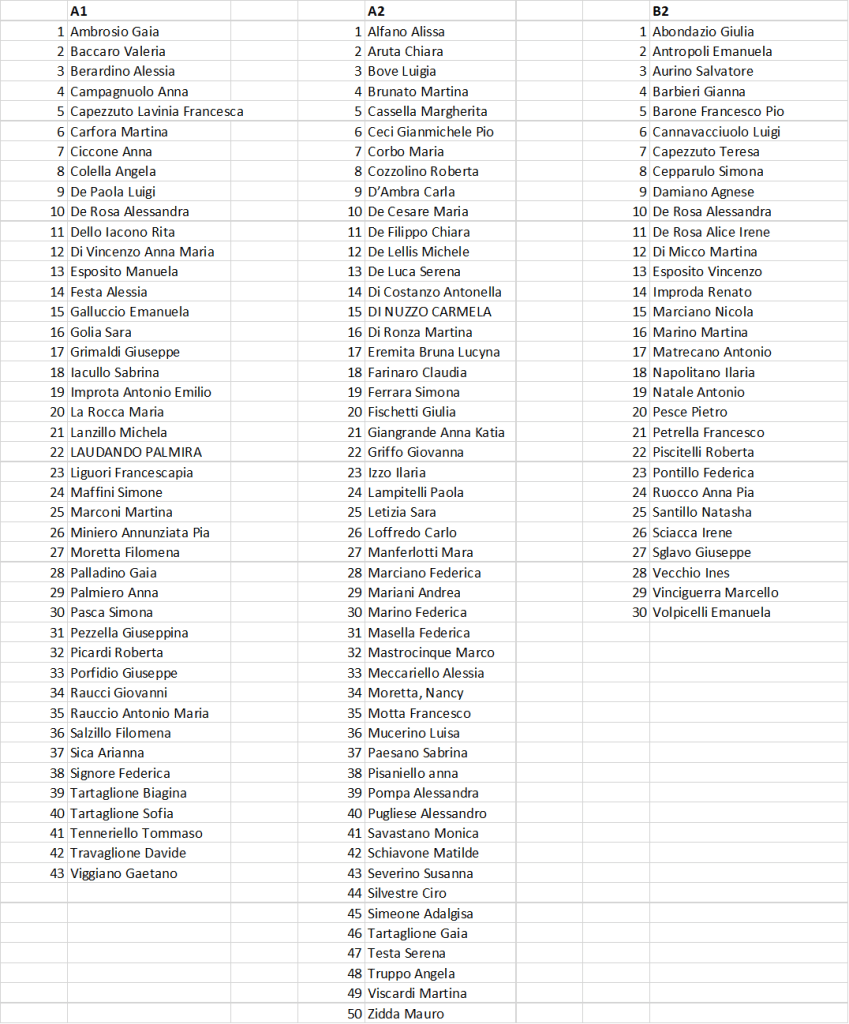
Qui troverete gli elenchi con la distribuzione nelle aule.
NB: tutti si considerano ammessi con riserva, in quanto sarà necessario verificare che siano stati rispettati gli obllighi di presenza
You must be logged in to post a comment.