Weekend Organic Chemistry Challenge

Regolamento:
- Vincerà la sfida chi risponderà per primo CORRETTAMENTE al seguente quesito
- La risposta dovrà essere inserita come commento al post. Per commentare è necessario essere registrati al blog ed aver effettuato il login! Identificarsi utilizzando nome e cognome.
- Ognuno può rispondere solo una volta (anche in presenza di più di un commento pubblicato dalla stessa persona, soltanto il primo sarà preso in considerazione).
- Il tempo massimo a disposizione sarà di 12h dalla pubblicazione del post.
- Il vincitore (3 punti) sarà annunciato lunedì a lezione.
Nella figura qui sotto sono riportati i due isomeri geometrici del cicloottene con i rispettivi valori del calore di idrogenazione. Possiamo notare che questi due composti rappresentano un’eccezione rispetto a quanto abbiamo imparato circa la stabilità degli alcheni.
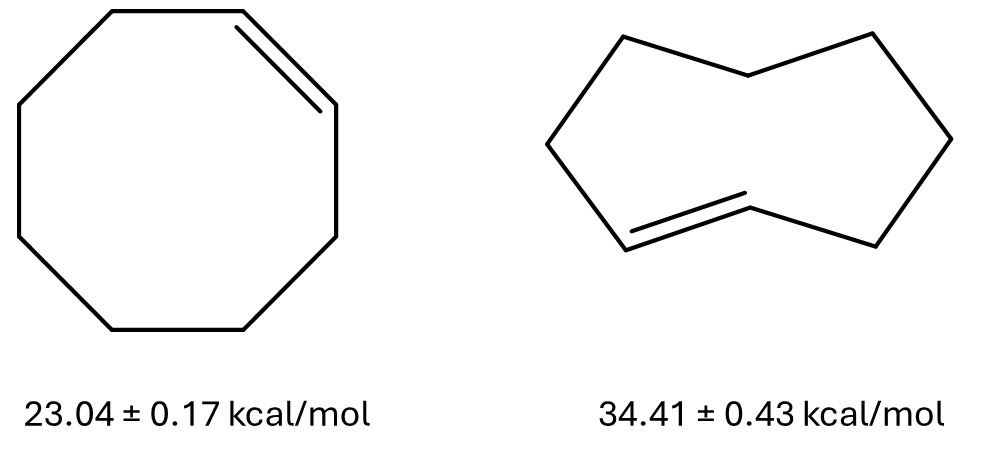
Fornire una spiegazione convincente di questi dati sperimentali.
NB: nella correzione delle risposte sarà valutato anche il corretto utilizzo della terminologia tecnica appropriata.
Abbiamo visto che per gli alcheni aciclici, quando si ha l’isomero cis, i sostituenti voluminosi si trovano dallo stesso lato del doppio legame causando tensione sterica nella molecola. Ciò rende l’isomero cis meno stabile, spiegando così il valore maggiore di calore di idrogenazione. Quando invece i sostituenti voluminosi si trovano da lati opposti, come nell’isola trans, le nuvole elettroniche non possono interagire e quindi non c’è interazione sterica, ottenendo così valori più bassi di calore di idrogenazione.
In questo caso specifico possiamo spiegare il risultato dei dati sperimentali confrontando la stabilità dell’isomero cis e trans per un ciclo a otto termini. L’isomero trans (quello di destra) presenta maggiore tensione torsionale, sterica e angolare a causa della conformazione che assume. Ciò destabilizza molto il composto, spiegando anche il maggiore calore di idrogenazione. L’isomero cis (quello di sinistra) presenta meno interazioni steriche, risultando così il conformero più stabile e con un calore di idrogenazione minore.
LikeLike
Nel caso del cicloottene l’eccezione è dovuta alla tensione ad anello.
A differenza degli alcheni ciclici nel cicloottene è l’isomero cis a risultare più stabile del trans, perché il cis riesce a posizionarsi in una conformazione senza troppi sforzi geometrici.
Mentre nell’esempio del trans, in un anello così piccolo, la catena deve forzarsi molto di più. Di conseguenza il trans-cicloottene ha un’energia più alta e sviluppa un calore di idrogenazione maggiore.
Bocchetti Francesco
Matricola: A36004745
LikeLike
Generalmente gli alcheni trans sono più stabili dei cis in quanto negli alcheni trans i gruppi più ingombranti si trovano più distanti tra di loro, mentre negli alcheni cis essendo questi gruppi più vicini tra loro destabilizzano la molecola. In questo caso il ciclo con una struttura trans é meno stabile proprio a causa della forma del ciclo che per restare una struttura in trans si deve piegare, l’anello subisce una distorsione , che porta anche all’aumento di interazioni steriche . Ecco perché l’energia liberata per il ciclo in trans é molto maggiore rispetto a quella che viene liberata per il ciclo in cis
Braccio Angela
A36004968
LikeLike
In generale più è stabile un alchene e minore sarà il suo calore di idrogenazione e in questo caso si potrebbe pensare che, avendo il cicloottene isomeria cis e il suo isomero geometrico isomeria trans, quest’ultimo sia più stabile, ma non è così.
Ciò è possibile a causa della maggiore tensione dell’isomero a destra, infatti possiamo dire che la struttura a destra va ad avere una maggiore tensione torsionale e una maggiore tensione angolare rispetto al cicloottene, rendendo la sua struttura meno stabile e, di conseguenza, maggiore il suo calore di idrogenazione.
Bianchi Chiara A36004958
LikeLike
Queste due figure rappresentano, la prima il cis-cicloottene e la seconda, il trans-cicloottene. Questi due isomeri geometrici presentano un diverso calore di idrogenazione: il cis, un calore di idrogenazione minore e il trans maggiore. Ricordiamo che il calore di idrogenazione è la quantità di energia che un alchene rilascia quando viene trasformato in un alcano, tramite idrogenazione catalitica. Se l’alchene rilascia più energia,(più calore di idrogenazione) allora è meno stabile, se rilascia meno energia (meno calore di idrogenazione) allora è più stabile. In questo caso in base ai valori riportati il cis è più stabile del trans. Un doppio legame ha una geometria planare fissa, cioè i due carboni sono ibridati sp2 e i tre legami stanno sul piano formando angoli di 120°. Inoltre il legame p greco richiede che gli orbitali p siano perfettamente paralleli, quindi parte dell’anello che contiene il doppio legame non può piegarsi liberamente. In particolare, in un alchene cis- i due sostituenti si trovano sullo stesso lato del doppio legame, mentre nel trans- a lato opposto. Nella geometria cis-, dunque, c’è poca tensione torsionale, proprio perchè i sostituenti si trovano sullo stesso lato. Mentre nel trans-, la struttura è deformata. Molte coppie di legami C-C sono eclissati, per cui aumenta la tensione torsionale e quindi l’energia. In un anello ad otto atomi, già piccolo e in cui è difficile disporre gli atomi in maniera da annullare la tensione, è quindi ancora più difficile la geometria trans. E’ questo, dunque, che determina la differenza di stabilità e quindi dei calori di idrogenazione dei due isomeri geometrici in questione.
LikeLike
A sinistra abbiamo l’isomero cis, mentre a destra invece l’isomero trans; generalmente l’isomero trans é quello più stabile (libera meno calore di idrogenazione), ma questo caso rappresenta un’eccezione perché la struttura dell’isomero trans determina tensione angolare e di conseguenza avremo una maggiore repulsione sterica, nel caso invece dell’isomero cis gli idrogeni dei carboni adiacenti si orientano in modo da massimizzare la sovrapposizione tra gli orbitali sigma C-H e l’obitale pi greco del doppio legame, favorendo quindi una maggiore delocalizzazione elettronica conferendo dunque una maggiore stabilità, di conseguenza verrà liberato meno calore di idrogenazione.
de Chiara Martina
A36004964
LikeLike
Domani scopriremo se qualcuno ha vinto la sfida. Intanto, qualche informazione su questo tipo di composti.
I trans-ciclootteni sono una classe di alcheni chirali planari che mostrano un’inaspettata reattività. Le loro caratteristiche strutturali sono state ampiamente studiate nella chimica organica fisica. Il trans-cicloottene esiste forma di due enantiomeri (atropoisomeri) e presenta un’elevata stabilità nei confronti della racemizzazione, con una barriera energetica di 35,6 kcal/mol. Questo composto può assumere, ovviamente, diverse conformazioni. La conformazione più stabile (“a corona”) presenta analogie strutturali con la conformazione a sedia del cicloesano, poiché i gruppi metilene in entrambe le conformazioni mostrano una disposizione alternata di idrogeni assiali ed equatoriali. Attenzione, però, questo non vuol dire che non ci siano tensioni in questo caso! Il doppio legame fortemente distorto determina uno stato energetico relativamente elevato dell’orbitale molecolare occupato di massima energia e rende questo composto molto reattivo. In virtù di questa reattività, trova applicazioni nella chimica bioortogonale (https://link.springer.com/article/10.1186/s41181-024-00275-x).
La chimica bioortogonale è un insieme di reazioni chimiche progettate per avvenire all’interno di sistemi biologici viventi senza interferire con i processi naturali delle cellule. Carolyn Bertozzi (Premio Nobel per la Chimica nel 2022) ha inventato questo approccio per marcare e studiare biomolecole (come i glicani sulla superficie cellulare) in cellule vive, senza danneggiarle. Le sue reazioni bioortogonali hanno rivoluzionato la biologia perché permettono, tra le altre cose, di tracciare molecole all’interno di cellule e organismi viventi, fare imaging senza tossicità, sviluppare nuove terapie e sistemi di rilascio mirato dei farmaci.
LikeLike