Weekend Organic Chemistry Challenge

Regolamento:
- Vincerà la sfida chi risponderà per primo CORRETTAMENTE al seguente quesito
- La risposta dovrà essere inserita come commento al post. Per commentare è necessario essere registrati al blog ed aver effettuato il login! Identificarsi utilizzando nome e cognome.
- Ognuno può rispondere solo una volta (anche in presenza di più di un commento pubblicato dalla stessa persona, soltanto il primo sarà preso in considerazione).
- Il tempo massimo a disposizione sarà di 12h dalla pubblicazione del post.
- Il vincitore (4 punti) sarà annunciato martedì a lezione.
La molecola mostrata in figura è il primo esempio di una molecola che contiene un ossigeno chirale, per cui è stato possibile sintetizzare e isolare un singolo enantiomero a temperatura ambiente (l’articolo relativo è stato pubblicato su Nature nel 2023).
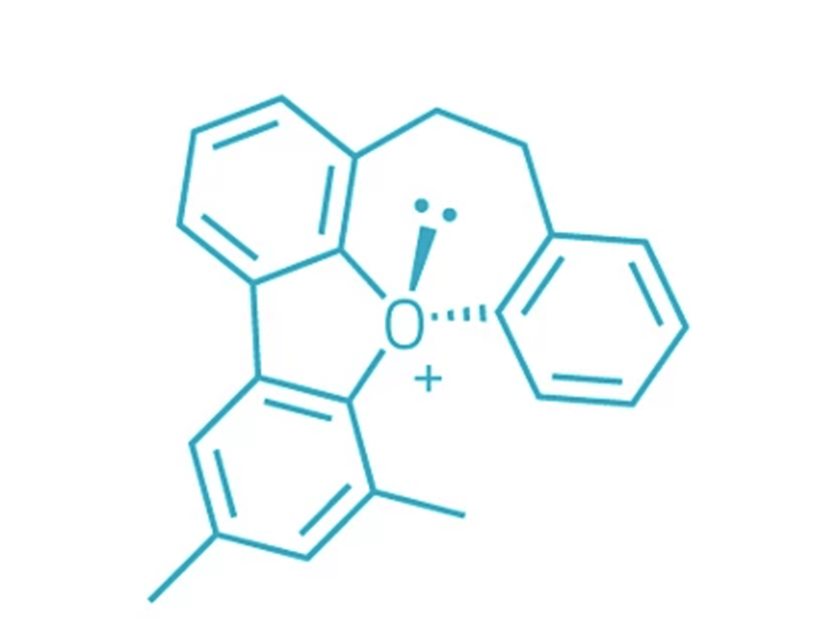
Infatti, sebbene il carbonio sia famoso per le sue capacità di formare centri chirali, abbiamo visto che anche altri atomi come fosforo, zolfo e azoto possono fungere da centri stereogenici nelle molecole organiche.
Gli ioni ossonio (come quello in figura), ossia composti che contengono un atomo di ossigeno con carica positiva legato a tre sostituenti, hanno il potenziale per essere chirali. In pratica, però, non è in genere possibile isolarne un singolo enantiomero a temperatura ambiente.
A) Spiegare sinteticamente perché non è possibile isolare la singola forma enantiomerica di uno ione ossonio, in generale.
B) Ipotizzare perché, invece, questo è stato possibile nel caso del composto mostrato in figura.
A) a causa della presenza della coppia solitaria sull’ossigeno, gli ioni ossonio possono interconvertire rapidamente nei due enantiomeri, siccome si passa attraverso uno stato di transizione in cui O è ibridato sp². Avendo quindi una geometria trigonale planare, i tre legami sono sul piano e si può avere sia l’uno che l’altro enantiomero. La barriera energetica da superare è molto bassa per cui si ha una rapida racemizzazione che rende impossibile separare gli enantiomeri.
B) Nel caso del composto illustrato, attorno all’atomo di ossigeno si ha molto ingombro sterico ed una certa rigidità dovuta alla struttura policiclica. Questi fattori impediscono la geometria planare necessaria per far avvenire l’inversione. La barriera energetica da superare diventa quindi piu alta, consentendo l’isolamento di un enantiomero
LikeLike
Non è possibile separare la singola forma enantiomerica perché la coppia solitaria di elettroni, a temperatura ambiente, interconverte rapidamente. Forse, in questo caso, è stato possibile perché questo composto è in grado di formare cristalli asimmetrici.
LikeLike
Santi Cristaudo A36004963
LikeLike
A) Solitamente non è possibile separare la forma enantiomerica di uno ione ossonio, perchè come nel caso del’inversione delle ammine gli enantiomeri interconvertono molto rapidamente a temperatura ambiente. L’ossigeno negli ioni ossonio è legato a tre gruppi R e ha una coppia solitaria mancante, per cui adotta una geometria piramidale. Durante l’inversione si passa attraverso uno stato in cui l’ossigeno ibridato sp3 diventa sp2. I tre legami O-R giacciono nello stesso piano, mediante i tre orbitali sp2, mentre rimane un orbitale p vuoto perpendicolare al piano. L’energia necessaria per tale inversione è piccola per cui a temperatura ambiente gli enantiomeri interconvertono rapidamente e per questo non possono essere separati.
B) In questo caso, probabilmente, l’ossigeno è inserito al centro di una serie di composti ciclici. I gruppi attorno all’ossigeno creano ingombro sterico, aumentando la barriera energetica per far sì che l’interconversione avvenga. Quindi in questo caso l’interconversione è più lenta ed è possibile isolare gli enantiomeri.
LikeLike
Non è possibile isolare la singola forma enantiomerica di uno ione ossonio perché uno dei gruppi legato all’ossigeno è una coppia solitaria, questo porta ad una rapida interconversione a temperatura ambiente delle due forme enantiomeriche.L’energia richiesta alla conversione da un enantiomero all’altra è molto bassa e dunque raggiungibile in modo facile a temperatura ambiente.
Probabilmente nella molecola in questione è stato possibile isolare la singola forma enantiomerica poiché osservando la struttura della molecola la coppia di elettroni non condivisa subisce ingombro sterico dalle nuvole elettroniche dei carboni che la “circondano” e questo probabilmente ostacola l’inversione di questo composto da una forma all’altra. L’energia necessaria per l’inversione del composto aumenta, la velocità con cui i due enentiomeri passano da una forma all’altra diminuisce notevolmente e dunque è stato possibile isolare le singole forme enantiomeriche.
LikeLike
È possibile che c’entri l’ibridazione: in questo caso nello ione ossonio l’ibridazione dovrebbe essere sp2 e il doppietto elettronico andrebbe ad occupare l’orbitale p, mentre i tre orbitali ibridi formano i tre legami con i carboni:
A) di solito non è possibile separare gli enantiomeri perché avendo un’ibridazione sp2 la geometria è trigonale planare ed essendo i sostituenti tutti sullo stesso piano gli enantiomeri non sono distinguibili.
B) in questo caso, però, lo ione ossonio è legato ad un ciclopentano, in cui la tensione angolare è abbastanza elevata da permettere un ripiegamento, il suo tipico ripiegamento a busta, che permette di dare un’orientamento spaziale ai sostituenti ed individuare così, meglio, i due enantiomeri del composto.
Gravante Rebecca Iolanda A36004999
LikeLike
Domani scopriremo l’eventuale vincitore della Challenge. Intanto, qui trovate la pubblicazione cui si fa riferimento: https://www.nature.com/articles/s41586-023-05719-z
LikeLike