Legami nei composti organici: esercizi su orbitali atomici, orbitali ibridi e orbitali molecolari

1. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

2. Indicare il tipo di ibridazione per ognuno degli atomi (escluso l’H) dei seguenti composti

3. Per gli atomi indicati da una freccia nei seguenti composti, indicare:

4. Descrivi ibridazione, geometria e angolo di legame per gli atomi indicati da freccia nella seguente struttura:
5a. Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

5b. In riferimento all’esercizio 5a, prendere in considerazione i legami presenti tra b/e e c/d rispettivamente. Fornire una descrizione dettagliata degli orbitali ibridi che si sovrappongono e degli orbitali molecolari che si formano.
6. Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
7. Gli orbitali molecolari di antilegame sono prodotti da:
a) interazione costruttiva (in fase) degli orbitali atomici
b) interazione distruttiva (fasi opposte) degli orbitali atomici
c) la sovrapposizione degli orbitali atomici di due ioni negativi
d) tutte le precedenti
e) nessuna delle precedenti
8. Quali orbitali ibridi si trovano nella molecola di acqua?
a) sp3
b) sp2
c) sp3d
d) sp
9. Quali orbitali si formano per sovrapposizione assiale di 2 orbitali sp3 ? Quali orbitali sono invece coinvolti nella formazione di un legame pi-greco?
10. Proporre formule di struttura per le molecole aventi le seguenti caratteristiche:
a) due atomi di carbonio ibridati sp2 e due atomi di carbonio ibridati sp3
b) quattro atomi di carbonio tutti ibridati sp2
c) due atomi di carbonio ibridati sp, e due atomi di carbonio ibridati sp2
11. Proporre la struttura di una molecole che soddisfi i seguenti criteri: contiene 2 atomi di carbonio ibridati sp2 e 2 atomi di carbonio ibridati sp3. Dire quali sono la geometria e gli angoli di legame di ciascun carbonio.
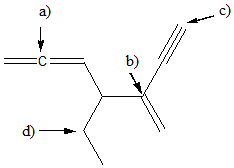
12. Nelle seguenti figure, alcuni dei legami sono indicati da freccia e da una lettera. a) Etichettare i legami a-d come singoli, doppi o tripli; b) Indicare (per quei legami) il tipo di orbitale/i molecolare/i; c) dire quali orbitali atomici/orbitali ibridi sono coinvolti nella formazione del legame.
d) Considerando tutti i legami singoli C-C della molecola, qual è il legame più corto? (NB: in questo caso ci riferiamo a tutti i legami, non solo a quelli indicati da freccia e lettera)
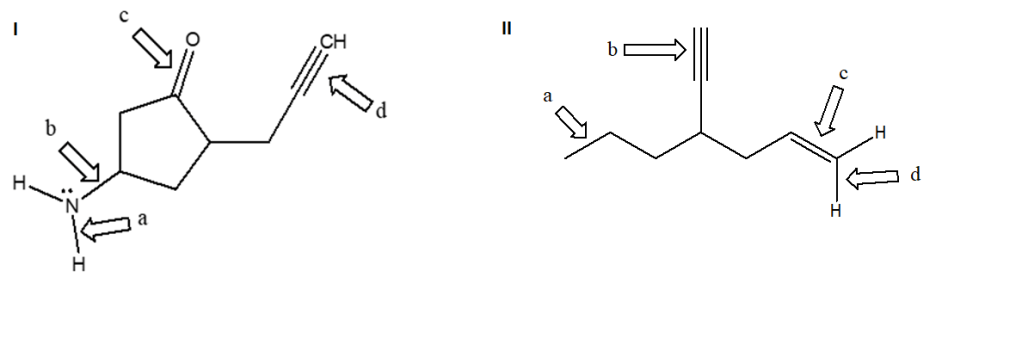
13. Nella seguente figura, alcuni dei legami sono indicati da freccia e da una lettera.

1) Etichettare i legami a-d come singoli, doppi o tripli;
2) indicare il tipo di orbitale/i molecolare/i;
3) dire quali orbitali atomici sono coinvolti nella formazione del legame.
4) Considerando tutti i legami singoli della molecola (ed escludendo i legami C-H) qual è il legame più corto?
14. Quella qui riportata è la struttura della vitamina C

a) Individuare il legame singolo C-C più corto
b) dire quali orbitali molecolari danno luogo al doppio legame C=O e quali orbitali atomici/ibridi sono usati per formare tali orbitali molecolari
c) dire quanti atomi di idrogeno in tutto sono presenti nella molecola
e) individuare gli atomi di carbonio ibridati sp2
15) La struttura di seguito riportata è quella della chinina. Osservare gli atomi e i legami indicati da lettere e numeri e completare le seguenti frasi o rispondere alle seguenti domande

I) La coppia solitaria dell’atomo di azoto a si trovano in un orbitale_______; quella dell’atomo di azoto b si trova in un orbitale_______
II) Osservare il legame indicato dalla c ed indicare il tipo di orbitale/i molecolare/i______________________________________________________________________________________
III) Quali orbitali atomici ibridi si sovrappongono per formare il legame c?_____________________________________________________________________________________
IV) Qual è il legame più corto tra quelli indicati dai numeri da 1 a 4?____________________________________________________________________________________
16. Il composto mostrato in figura è il paclitaxel, un farmaco antitumorale. Indicare l’ibridazione dei carboni indicati dalle lettere A e B e dai numeri 1,2,3.

17. Dire quali sono l’ibridazione, la geometria e l’angolo di legame del catione metile.
18. Dire com’è ibridato l’atomo di ossigeno nella molecola d’acqua. Dire quali sono le evidenze a favore di tale ibridazione.
Qui è possibile scaricare le soluzioni https://drive.proton.me/urls/QETQXWB37R#Q1jrmRlRfUXD. La password è stata comunicata a lezione
LikeLike