Acidi e basi II

1) Scrivi i prodotti delle seguenti reazioni acido-base e indica la direzione dell’equilibrio

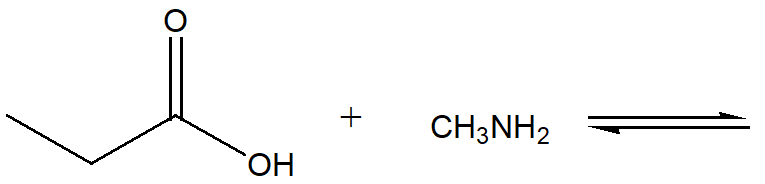
2) Rispondere ai seguenti quesiti:
a) A quale valore di pH la concentrazione della forma basica di un composto con pKa 6.2 è 100 volte maggiore rispetto alla forma acida?
b) A quale valore di pH la concentrazione della forma acida di un composto con pKa 3.4 è 10 volte maggiore rispetto alla forma basica?
c) A quale valore di pH il 50% di un composto con pKa 7.2 si troverà in soluzione nella forma basica?
(PRIMA di svolgere questo esercizio, si consiglia di consultare il problema risolto presente sul libro a pagina 73-problema 44).
3) Per ciascuno dei seguenti composti, scrivi la forma predominante a pH 3; 6; 10; 14
CH3CH2OH (pKa= 15,9)
CH3COOH (pKa= 4,8)
CH3CH2NH3+ (pKa= 11,0)
4) Dire quale atomo nella seguente molecola può essere più facilmente deprotonato

5) Metti i seguenti composti in ordine di acidità crescente e motiva la scelta
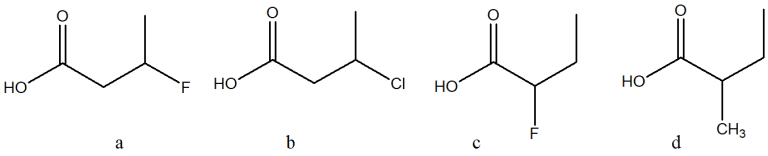
6) Mettere gli acidi alogenidrici in ordine di acidità decrescente, motivando la scelta.
7) Disporre i seguenti composti in ordine di basicità decrescente (dal più basico al meno basico) e spiegare sinteticamente il perché:

8) Cerchiare l’acido più debole e motivare sinteticamente la scelta.
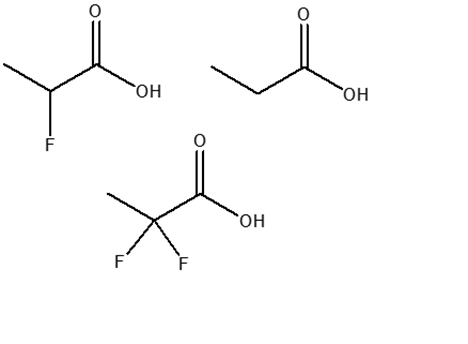
9) Cerchiare la base più forte e motivare sinteticamente la scelta.

10) Elencare i seguenti idrogeni in ordine di acidità crescente (dal valore più basso a quello più alto) e motivare la scelta
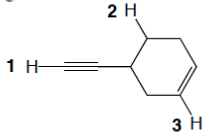
Per gli esercizi 1-5 è possibile vedere https://chimicaorganicadistabif.com/2022/10/10/acidi-e-basi-ii/
In assenza di un mio commento, è possibile che gli esercizi non siano stati corretti (per cui prendete solo in considerazione i commenti in cui vedete una mia correzione!)
Gli altri esercizi sono stati affrontati (o sono molto simili a quelli affrontati) alle esercitazioni. Se qualcuno ha dubbi, può commentare qui (o contattare la docente) e riceverà l’eventuale correzione
LikeLike