Alcune rappresentazioni della struttura di un composto organico: esercizi

1) Scrivere la struttura di Lewis dello ione solfato. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza. Calcolare le cariche formali di ciascun atomo.
2) Per lo ione fosfato (PO43-) è possibile scrivere diverse strutture di risonanza. Scrivere la struttura di Lewis che rappresenta una delle strutture che contribuisce maggiormente all’ibrido di risonanza. Calcolare le cariche formali per tutti gli atomi.
3) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di carbonio e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza
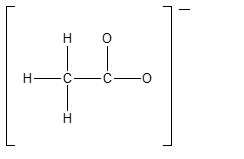
4) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di zolfo e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza.

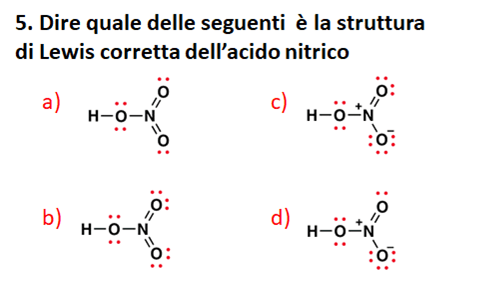
5) Tra le strutture riportate di seguito, solo una rappresenta in maniera corretta il composto di formula molecolare C2H5OH. Individuare la struttura corretta e individuare gli errori presenti nelle altre.
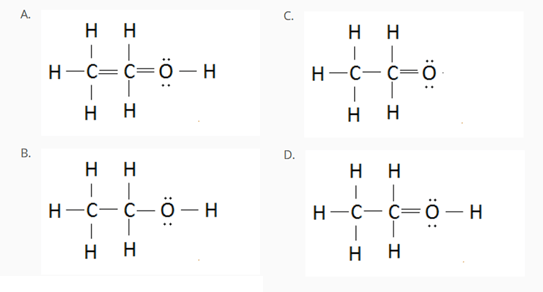
6) Disegnare la struttura di Lewis del composto di formula molecolare CH2Br2
7) Scrivere una formula condensata, la formula molecolare e la struttura a segmenti per ciacuna delle seguenti strutture di Kekulé
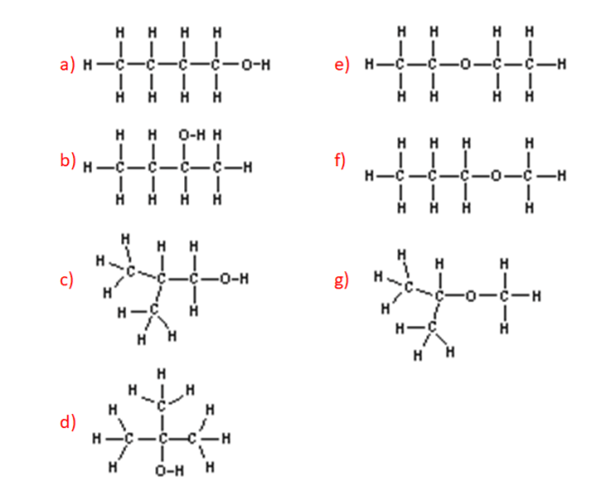
8) Scrivere la struttura di Kekulé, la formula molecolare e la struttura a segmenti per ciacuna delle seguenti formule condensate

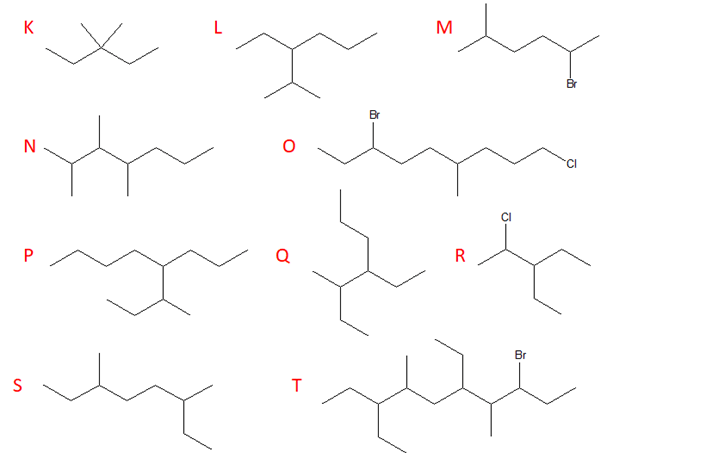
9) Per ciascuna delle seguenti strutture a segmenti, scrivere una formula condensata, la struttura di Kekulé corrispondente e la formula molecolare

10) Per ciascuno dei seguenti composti, scrivi a) formula molecolare, b) struttura di Kekulè, c) una struttura condensata alternativa, quando possibile d) la struttura a segmenti

11) Disegna la struttura a segmenti per ciascuno dei seguenti composti

12) Scrivi una delle possibili strutture condensate per ciascuno dei seguenti composti
















You must be logged in to post a comment.