Training I

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomenti…e a breve altre liste di domande saranno pubblicate. In ogni caso, potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti. In fondo alla lista, troverete anche una classifica del livello di difficoltà delle domande.
- Fornire una definizione di composto aromatico.
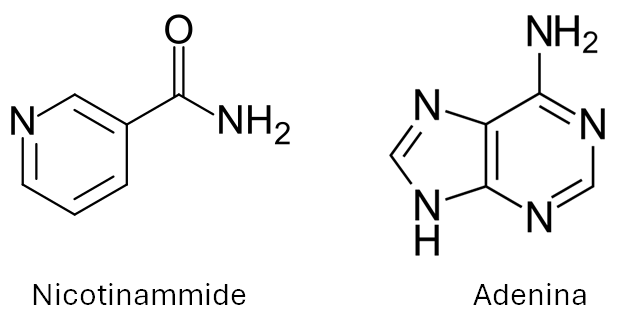
- La nicotinammide (o niacinammide), mostrata alla fine del post, è una piridina sostituita. Si tratta o meno di un composto aromatico?
- Spiegare cosa si intende per energia di risonanza o di delocalizzazione.
- Concentriamoci ora sul gruppo funzionale ammidico presente nella nicotinammide. Cosa possiamo dire circa: a) ibridazione deli atomi coinvolti; b) lunghezza dei legami e forza dei legami; c) geometria molecolare; d) reattività del gruppo funzionale.
- Cosa succede se mettiamo il gruppo funzionale ammidico in presenza di LiAlH4? (Definire solo il tipo di reazione!)
- Anche l’adenina (la cui struttura è mostrata alla fine del post) è un composto aromatico. Spiegare perchè.
- Su ciascun atomo di azoto della base azotata in questione è presente una coppia solitaria di elettroni. Dire, per ciascun atomo di azoto, in che tipo di orbitali si trova tale coppia solitaria.
- A proposito di composti aromatici, non si può non parlare del benzene. Nella reazione del benzene con Br2 è necessario utilizzare un catalizzatore. a) quale catalizzatore? b) perchè dobbiamo usare un catalizzatore? c) che tipo di reazione avviene? d) mostrare il meccanismo; e) confrontare questa reazione con quella di Br2 con il 2-butene.
- A partire da uno degli isomeri del 2-butene, sintetizzare il 2-metil-2-butene. Potrebbero essere necessari più passaggi. Indicare strategia sintetica, condizioni di reazione e meccanismi (se questi ultimi sono tra quelli che dovete conoscere).
- Far reagire il 2-metil-2-butene con a) HBr; b) Br2 in CH2Cl2; c) Br2 in CH3OH; d) 9-BBN e facendo seguire una reazione di ossidazione; e) un perossiacido. Per tutti, mostrare il meccanismo e la stereochimica dei prodotti (NB: è necessario mostrare gli aspetti stereochimici contestualmente al meccanismo).
- Disegnare il diagramma dell’energia libera vs la coordinata di reazione per la reazione 10a. Indicare sul grafico reagenti, prodotti, stato di transizione e intermedi di reazione.
- L’intermedio della reazione precedente (quella della domanda 11) è un carbocatione. Stabilire un ordine di stabilità per i carbocationi primari, secondari, terziari e argomentare.
- Dire cosa succede se mettiamo i seguenti composti in metanolo: 1-bromobutano, 1-bromo-1-butene, 1-bromo-2-butene. Argomentare la risposta.
- Se mettiamo l’1-bromobutano in presenza di ione idrossido quale sarà il prodotto principale? A partire dal prodotto ottenuto, cosa si ottiene se si fa reagire con PCC? Il prodotto di questa seconda reazione ha idrogeni acidi? Perchè?
- Per il/i composto/i sintetizzato/i in 10d, disegnare la proiezione di Newman lungo il legame C2-C3 del conformero più stabile.
- Spiegare perchè i conformeri eclissati sono meno stabili dei conformeri sfalsati.
- A partire da uno dei composti sintetizzati in 10e, sintetizzare il 2,3-dimetil-2,4-esadiene. Potrebbero essere necessari più passaggi. Indicare strategia sintetica, condizioni di reazione e meccanismi (se questi ultimi sono tra quelli che dovete conoscere). Seguire sempre la stereochimica nel corso della reazione. Spiegare perchè il prodotto ottenuto sarà il prodotto principale.
- Parlando ora di nuovo dell’adenina della domanda 6, si tratta di una delle basi azotate che costituiscono una delle unità strutturali dei nucleotidi. Quali sono gli altri componenti strutturali di un nucleotide? E di un nucleoside?
- Nel caso dell’adenosina, un nucleoside, il ribosio presente in questa molecola è o meno uno zucchero riducente? Perchè?
- Scrivere il D-ribosio nella forma a catena aperta, sapendo che si tratta di un aldopentoso e che la configurazione assoluta dei carboni 2 e 3 è R.
- Scrivere l’L-ribosio
- Scrivere il prodotto del D-ribosio con sodio boro idruro
- L’alditolo ottenuto in 22 non è otticamente attivo. Spiegare perchè.
- Partendo dal D-ribosio, effettuare una sintesi di Kiliani-Fisher.
- Dalla 24 si ottengono D-allosio e D-altrosio. Perchè si ottengono due prodotti?
- Che tipo di reazione è la prima che si usa in 24?
- Nell’ultimo passaggio della sintesi in 24 l’immina formata viene idrolizzata. Parlando di immine in generale, perchè mentre la reazione di sintesi è reversibile, quella di idrolisi non lo è nelle condizioni in cui viene effettuata?
- Tornando al D-ribosio, quale sarà il prodotto della sua reazione col reattivo di Tollens?
- Nel prodotto ottenuto in 28 c’è uno dei legami singoli C-O che è più corto rispetto agli altri. Dire quale e spiegare perchè. Spiegare anche perchè l’idrogeno del gruppo carbossilico è più acido di quello del gruppo ossidrile.
- Il ribosio può essere ossidato a dare un acido aldonico anche utilizzando acqua di bromo (Br2 in acqua). Il chetoso corrispondente, il ribulosio, può essere ossidato a dare lo stesso acido aldonico (più un altro prodotto) solo col reattivo di Tollens e non con acqua di bromo. a) Spiegare perchè; b) spiegare perchè otteniamo due prodotti; c) quanti prodotti otteniamo quando ossidiamo il ribosio con reattivo di Tollens?
Grado di difficoltà delle domande:
Alto (richiedono più passaggi e/o notevole padronanza della disciplina): 9, 17
Medio (domande che vanno al di là della mera esposizione/applicazione di concetti teorici): 6, 8, 14, 20, 24, 25, 29, 30
Basso (domande che riguardano l’esposizione di concetti teorici, la dimostrazione di semplici meccanismi di reazione, l’applicazione diretta di concetti teorici di base): tutte le domande non incluse nelle due liste precedenti.
You must be logged in to post a comment.