Esercitiamoci ancora un po’ per la prima prova intercorso

1) Proporre la struttura di una molecole che soddisfi i seguenti criteri: contiene 2 atomi di carbonio ibridati sp2 e 2 atomi di carbonio ibridati sp3. Dire quali sono la geometria e gli angoli di legame di ciascun carbonio.
2) Scrivere la struttura di Lewis dello ione solfato. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza. Calcolare le cariche formali di ciascun atomo.
3) Rispondere ai seguenti quesiti:
a) A quale valore di pH la concentrazione della forma basica di un composto con pKa 5.2 è 100 volte maggiore rispetto alla forma acida?
c) A quale valore di pH il 50% di un composto con pKa 6.4 si troverà in soluzione nella forma basica?
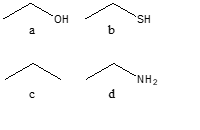
4) Disporre i seguenti composti in ordine di acidità decrescente e spiegare sinteticamente il perché:
a) CH3CH2CH2SH b) CH3CH2CH2NH2 c) CH3CH2CH2CH3 d) CH3CH2CH2OH
5) Attribuire il nome IUPAC ai seguenti composti
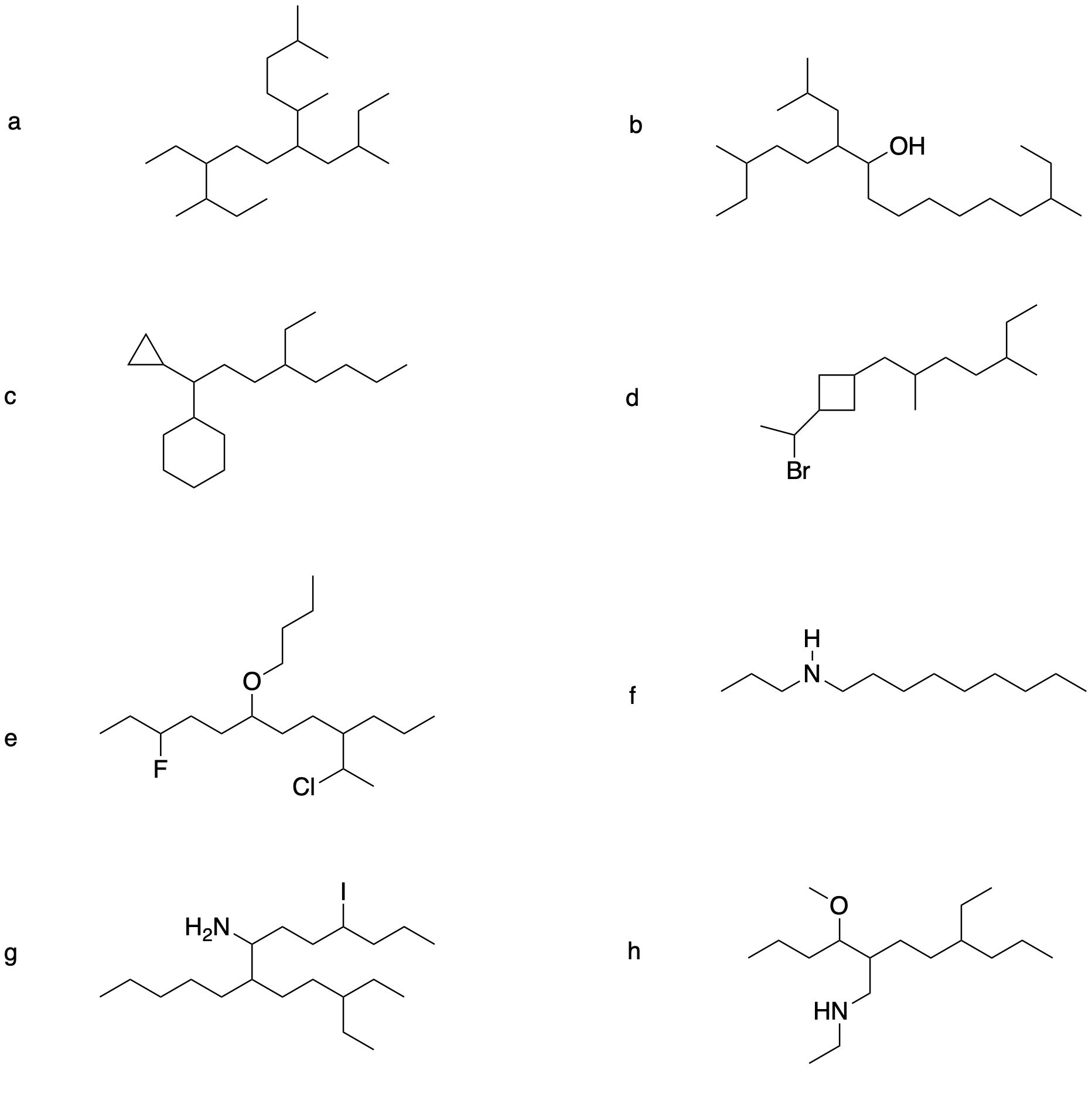
6) Rappresentare la struttura a segmenti e attribuire il nome IUPAC ad un composto di formula molecolare C10H20 che contiene solo H primari e terziari.
7) Quella qui riportata è la struttura della vitamina C

a) Individuare il legame C-C più corto
b) dire quali orbitali molecolari danno luogo al doppio legame C=O e quali orbitali atomici/ibridi sono usati per formare tali orbitali molecolari
8) Dire quali sono l’ibridazione, la geometria e l’angolo di legame del catione metile.
9) Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
e) può essere sia di legame sia di antilegame
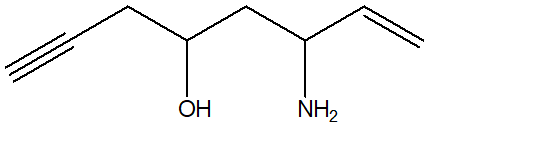
10) Dire quale atomo nella seguente molecola può essere più facilmente deprotonato
11) Metti i seguenti composti in ordine di basicità crescente e motivare la scelta

12) Scrivi il prodotto della seguente reazione acido-base e indica la direzione dell’equilibrio
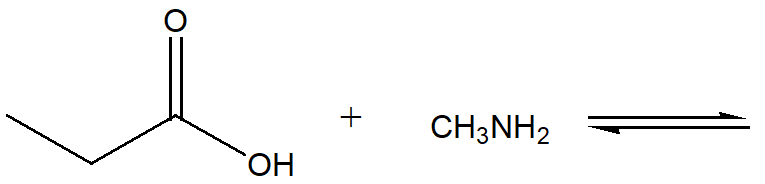
13) Disegnare il 4-etil-2-isopropil-1-metilcicloeano e dire se il nome IUPAC è corretto. Se non lo è, apportare le opportune correzioni.
14) Mettere gli acidi alogenidrici in ordine di acidità decrescente, motivando la scelta.
15) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di zolfo e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza. (1pt)
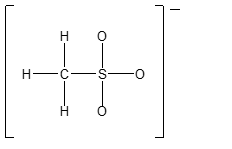
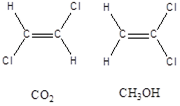
16) Cerchiare la/le molecola/e che ha/hanno momento dipolare nullo. (1 pt)
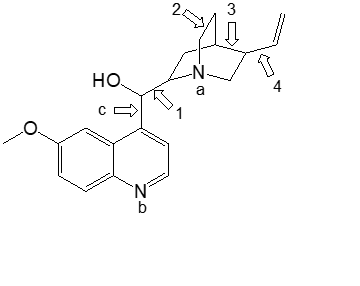
17) La struttura di seguito riportata è quella della chinina. Osservare gli atomi e i legami indicati da lettere e numeri e completare le seguenti frasi o rispondere alle seguenti domande
(4 pt)
I) La coppia solitaria sull’atomo di azoto a si trova in un orbitale_______; quella sull’atomo di azoto b si trova in un orbitale_______
II) Osservare il legame indicato dalla c e indicare il tipo di orbitale/i molecolare/i:
_____________________________________________________________________________________
III) Quali orbitali atomici si sovrappongono per formare il legame c?
_____________________________________________________________________________________
IV) Qual è il legame più corto tra quelli indicati dai numeri da 1 a 4? _______________________________________________________________________________________
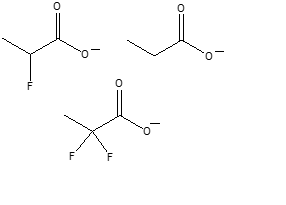
18) Disporre i seguenti composti in ordine di acidità crescente (dal meno acido al più acido) e spiegare sinteticamente il perché: (2pt)
19) Completare la reazione e dire dove è spostato
il seguente equilibrio (1 pt)
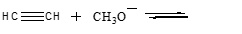
20) Cerchiare la base più forte e motivare sinteticamente la scelta. (2 pt)
21) Scrivere e attribuire il nome IUPAC al composto di formula C9H18 che possiede solo idrogeni primari. (2pt)
22) Disegnare il 4-etil-2-isopropil-1-metilcicloeano (1pt)
23) Scrivere la formula condensata di un isomero strutturale del 2,3-dimetilpentano (2pt)
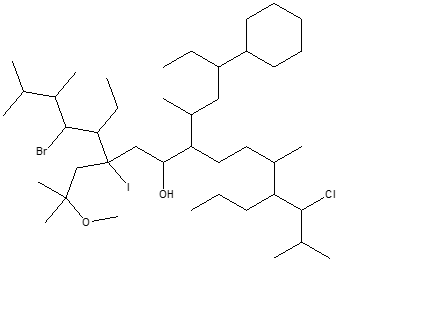
24) Assegnare il nome IUPAC ai seguenti composti:
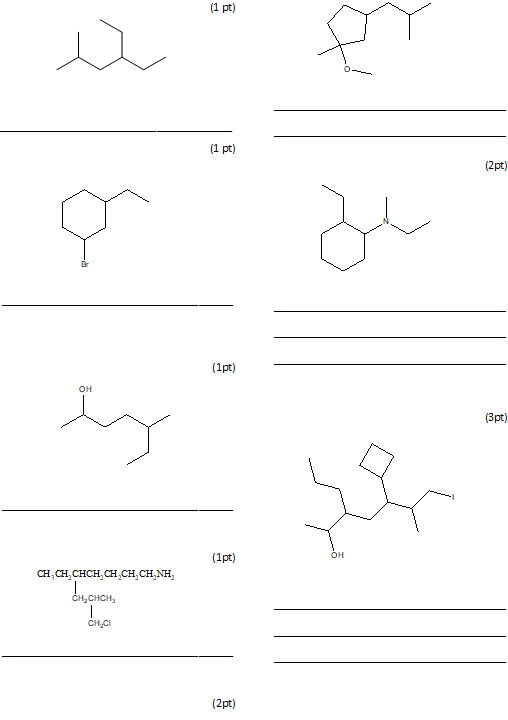
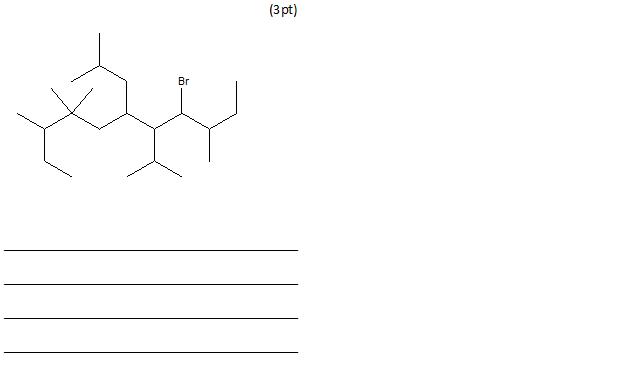
Denominare il seguente composto secondo le regole del sistema di nomenclatura IUPAC (4pt)
Nell’esercizio 24…l’ultimo esercizio è 8-bromo-3,4,4,9-tetrametil-7-(1-metiletil)-6-(2-metilpropil)undecano?
Comincio a numerare da sinistra perché in posizione 4 ho due metili? Il “dimetil” in posizione 4 vale come due? quando scelgo la direazione noto che da destra il terzo sostituente sarebbe in posizione 5,mentre da sinistra se considero i mitili sulla stessa posizione due sostituenti allora ho il terzo sostituente in posizione 4 e comincio da lì?
LikeLike