Legami nei composti organici: esercizi su orbitali atomici, orbitali ibridi e orbitali molecolari

1. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

2. Indicare il tipo di ibridazione per ognuno degli atomi (escluso l’H) dei seguenti composti

3. Per gli atomi indicati da una freccia nei seguenti composti, indicare:

4a. Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

4b. In riferimento all’esercizio 4a, prendere in considerazione i legami presenti tra b/e e c/d rispettivamente. Fornire una descrizione dettagliata degli orbitali ibridi che si sovrappongono e deli orbitali molecolari che si formano.
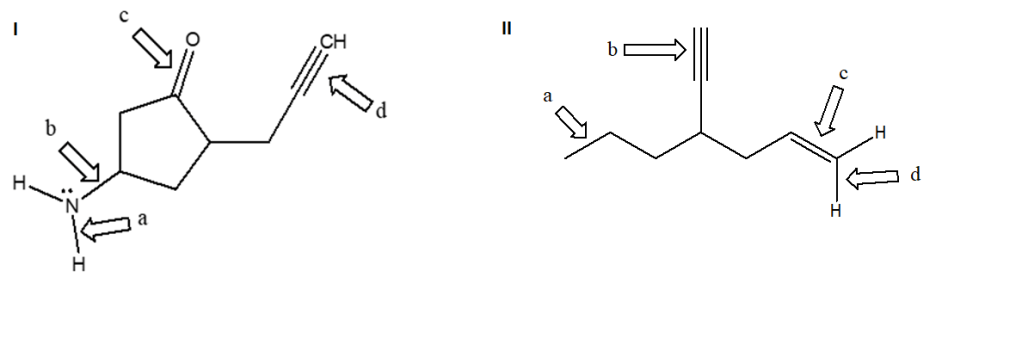
5. Nelle seguenti figure, alcuni dei legami sono indicati da freccia e da una lettera. a) Etichettare i legami a-d come singoli, doppi o tripli; b) Indicare (per quei legami) il tipo di orbitale/i molecolare/i; c) dire quali orbitali atomici/orbitali ibridi sono coinvolti nella formazione del legame.
d) Considerando tutti i legami singoli della molecola (ed escludendo i legami C-H) qual è il legame più corto? (NB: in questo caso ci riferiamo a tutti i legami, non solo a quelli indicati da freccia e lettera)
6. Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
e) può essere sia di legame sia di antilegame
7. Gli orbitali molecolari di antilegame sono prodotti da:
a) interazione costruttiva (in fase) degli orbitali atomici
b) interazione distruttiva (fasi opposte) degli orbitali atomici
c) la sovrapposizione degli orbitali atomici di due ioni negativi
d) tutte le precedenti
e) nessuna delle precedenti
8. Quali orbitali ibridi si trovano nella molecola di acqua?
a) sp3
b) sp2
c) sp3d
d) sp
9. Proporre formule di struttura per le molecole aventi le seguenti caratteristiche:
a) due atomi di carbonio ibridati sp2 e due atomi di carbonio ibridati sp3
b) quattro atomi di carbonio tutti ibridati sp2
c) due atomi di carbonio ibridati sp, e due atomi di carbonio ibridati sp2
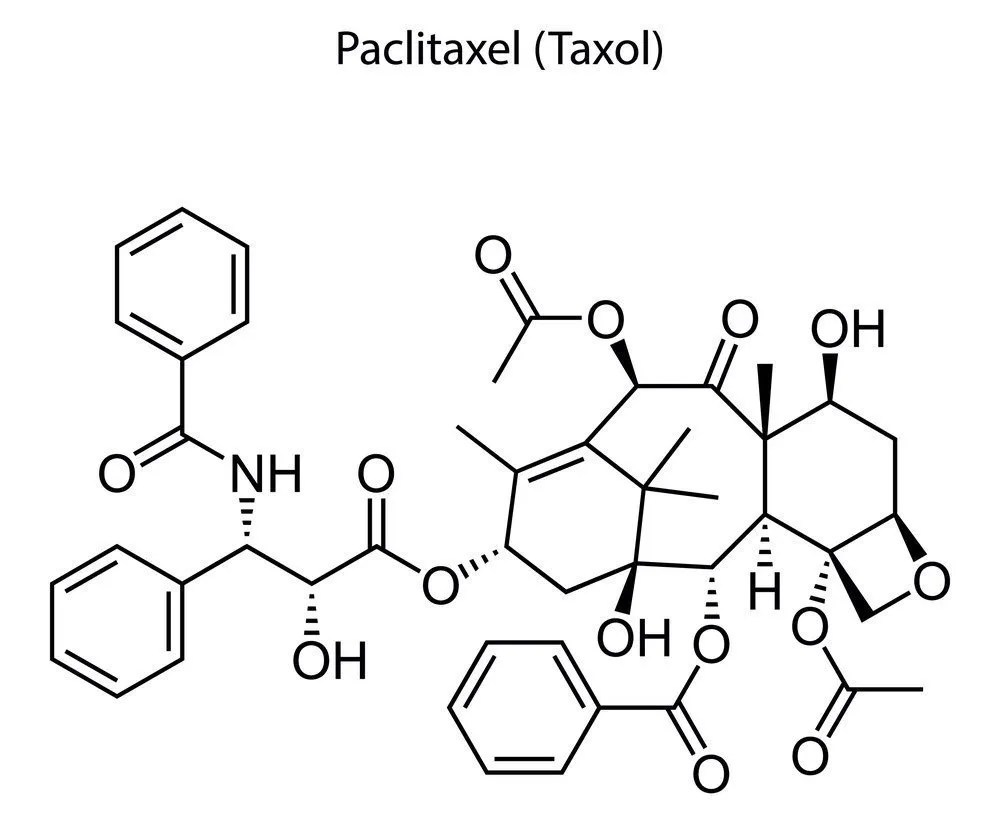
10. Di seguito è riportata la strutturara del Paclitaxel, un farmaco antitumorale di origine naturale. Definire l’ibridazione di tutti gli atomi (esclusi gli atomi di idrogeno). Ricordate che gli idrogeni legati al carbonio non sono esplicitati.
Esercizio 1
A) orbitale atomico p
B) orbitale atomico sp2
C) orbitale molecolare π
D) orbitale molecolare σ*
E) orbitale atomico p
F) orbitale atomico sp
G) orbitale atomico p lungo l’asse x
ESERCIZIO 2
-Primo composto ( da sinistra a destra)
C sp3
C sp3
N sp3
C sp2 ( quello con doppio legame )
C sp2 ( con il doppio legame )
-secondo composto ( da sinistra a destra)
C sp ( quello con legame triplo )
C sp ( con legame triplo)
C sp2 ( con legame doppio )
C sp2 ( con legame dpppio)
C sp3
Cl sp3
-terzo composto
N sp
C sp
C sp3
C sp2 ( quello con doppio legame )
C sp2 ( quello con doppio legame)
C sp3
C sp3
C sp2 ( quello che lega l’ossigeno)
O sp2
C sp3
ESERCIZIO 3
Primo composto:
A) 2 doppietti elettronici non condivisi
B) sp3
C) tetraedrica
D) < 104,5
Secondo composto
CH
A) 0 doppietti elettronici non condivisi
B) sp2
C) trigonale planare
D) 120
CH3
A) 0 doppietti elettronici non condivisi
B) sp3
C) tetraedrica
D) 109,5
Terzo composto
A) 0 doppietti elettronici non condivisi
B) sp2
C) trigonale planare
D)120
ESERCIZIO 4 a
A) sp3
B) sp3
C) sp
D) sp
E) sp2
F) sp2
ESERCIZIO 4b
Il legame c/d presenta un legame triplo tra due C entrambi ibridati sp3 con la formazione, a seguito della loro sovrapposizione, di due orbitali molecolari π ed uno σ. Gli orbitali sp sono costituiti da un s ed uno p che si ibridano per formare 2 orbitali sp che sono disposti in direzioni opposte con un angolo di legame di180 gradi. Essendo però che l’orbitale p è costituito da tre orbitali degeneri e solo uno è utilizzato nella formazione degli orbitali ibridi sp, i due non ibridati rimanenti saranno posti perpendicolarmente agli orbitali sp. Nella sovrapposizione per la formazione del triplo legame carbonio-carbonio si avrà che:
-dalla sovrapposizione degli orbitali sp si formerà un un orbitale molecolare σ
-la sovrapposizione laterale dei 4 orbitali P non ibridati appartenente ai due carboni formeranno 2 orbitali molecolari π.
Nel legame B/e si ha un legame singolo tra un carbonio ibridato sp3 ed uno ibridato sp2 la cui sovrapposizione porterà alla formazione di un orbitale molecolare σ.
L’orbitale ibrido sp3 è formato dall’orbitale S ed i tre orbitali degeneri P che si combinano tra loro e formano quattro orbitali sp3 aventi geometria tetraedrica.
L’orbitale ibrido sp2 è formato dall’orbitale s e dall’orbitale P il quale utilizza solo due dei suoi orbitali degeneri per formare tre orbitali sp2, mentre, il terzo orbitale degenere p è posto perpendicolarmente al piano. L’ibridazione sp2 genera così una geometria trigonale planare.
La sovrapposizione degli orbitali sp3 con sp2 genera solo un orbitale molecolare σ. In quanto il C che ha ibridazione sp3 non ha orbitali p non ibridati da poter usare per formare legami π.
ESERCIZIO 5
Primo:
A singolo, 1 σ, sp3/s
B singolo, 1 σ, sp3/sp3
C doppio, 1 σ 1 π, sp2/sp2 p/p
D triplo, 1 σ 2 π, sp/sp p/p p/p
Il legame più corto C-C dove c’è il triplo legame
Secondo
A singolo, 1 σ, sp3/ sp3
B triplo, 1 σ 2 π, sp/sp p/p p/p
C doppio 1 σ 1 π, sp2/sp2 p/p
D singolo 1 σ, sp2/s
Il legame più corto è dove c’è la lettera B
ESERCIZIO 6
A
ESRCIZIO 7
B
ESERCIZIO 8
A
ESERCIZIO 9
A) CH3-CH=CH-CH3
B) CH2=CH-CH=CH2
C) CH2=CH-C=-CH (=- sarebbe legame triplo)
LikeLike
Esercizio 3, fai attenzione alla geometria delle molecole quando l’atomo centrale contiene doppietti elettronici non condivisi. Rivedi la struttura della molecola d’acqua e ricontrolla la geometria del primo composto.
Per quanto riguarda l’esercizio 4b, dovresti cercare di essere più sintetica e chiara nella risposta. Alcuni concetti non sono espressi in maniera corretta. Es: l’orbitale p NON è costituito da tre orbitali degeneri, ma ogni livello contiene tre orbitali p degeneri… Esprimere i concetti in maniera corretta e utilizzare il linguaggio tecnico adeguato è essenziale
LikeLike
1)
a=orbitale atomico p
b=orbitale sp2 atomico
c=orbititale molecolare pi greco
d=orbitale molecolre di antilegame sigma star
e=orbitale atomico p
f=orbitale atomico sp
g=orbitale atomico s
2)Partendo da sinistra verso destra nel primo composto:il primo carbonio sp3,il secondo sp3,il terzo sp2,il quarto sp2. L’azoto sp3.
Nel secondo composto partendo da sinistra verso destra:il primo carbonio sp,il secondo sp,il terzo sp2,il quarto sp2,il quinto sp3. Il cloro sp3
Nel terzo composto:l’azoto sp. Partendo da sinistra verso destra:il primo carbonio sp,il secondo sp3,poi continuando verso l’alto sp2,poi sp2,poi sp3.Il carbonio che chiude il ciclo è sp3. Il carbonio che lega l’ossigeno è sp2,l’ossigeno sp2 e il carbonio rimanente è sp3.
3)Nel primo composto:
a=2
b=sp3
c=tetraedrica
d=104,5
Nel secondo composto il carbonio in alto:
a=0
b=sp2
c=trigonale planare
d=120
Il carbonio in basso:
a=0
b=sp3
c=tetraedrica
d)104,5
Nel terzo composto
a=0
b=sp2
c=trigonale planare
d=120
4A)
a=sp3
b=sp3
c=sp
d=sp
e=sp2
f=sp2
4B)Il legame b/e è un legame singolo. Si ha la sovrapposizione tra un orbitale atomico sp3 è uno sp2 con formazione di un orbitale molecolare sigma.
Il legame c/d è un legame triplo. Il carbionio D lega il carbonio E con la formazione di un orbitale molecolare sigma dovuto alla sopvrapposizuone tra l’orbitale molecolare sp-sp e due orbitali molecolari pi greco dovuti alla sovrapposizione p-p per la formazione del terzo e del secondo legame.
5)A Nel primo composto:
a=singolo
b=singolo
c=doppio
d=triplo
Nel secondo composto:
a=singolo
b=triplo
c=doppio
d=singolo
B Nel primo composto:
a=sigma
b=sigma
c=sigma e pi greco
d=1 sigma e due pi greco
Nel secondo composto:
a=sigma
b=1 sigma e due pi prego
c=1 sigma e 1 pi greco
d=sigma
C Nel primo composto
a=sp3-s
b=sp3-sp2
c=il sigma sp2-sp2
il pi greco p-p
d=il sigma sp-sp
pi greco p-p
Nel secondo composto
a=sp3-sp3
b=sigma sp-sp
pi greco p-p
c=sigma sp2-sp2
pi greco p-p
d=sp2-s
D Il legame più corto in entrambi i composti è il legame carbonio carbonio che precede il triplo legame.
6)A
7)B
8)A
LikeLike
Esercizio 3: anche per te vale il commento fatto alla tua collega. Nel tuo caso, però, devi anche ricontrollare qual è il valore dell’angolo tetraedrico.
Esercizio 4b: La risposta non è completa
Esercizio 5) controlla la risposta c per la lettera b del primo composto
LikeLike
ESERCIZIO 1
a) orbitale atomico p
b) orbitale atomico sp2
c) orbitale molecolare pigreco
d) orbitale molecolare antilegame sgmastar
e) orbitale atomico p
f) orbitale molecolare sp
g) orbitale atomico s
ESERCIZIO 2
Primo composto (da sinistra a destra): sp3,sp3,sp2,sp2 (N sp3)
Secondo composto (da sinistra a destra): sp,sp,sp2,sp2,sp3 (Cl sp3)
Terzo composto (da sinistra a destra): sp, sp3,sp2,sp2,sp3,sp3,sp2,sp3 (Nsp, Osp2)
ESERCIZIO 3
Primo composto:
a) due doppietti non condivisi
b) sp3
c) geometria angolata derivante a quella tetraedrica
d)104.5°
Secondo composto:
a) nessun doppietto non condiviso
b) sp2, sp3
c) geometria trigonale planare, tetraedrica
d)120°, 109,5°
a) un doppietti non condivisi
b) sp3
c) geometria trigonale planare
d)120°
ESERCIZIO 4a
a) sp3; b)sp3; c)sp; d)sp; e)sp2; f)sp2
ESERCIZIO 4Bb
LEGAME D/E
Il carbonio “d” è ibridato sp3 e instaura con il carbonio “e” ibridato sp2, un legame sigma. L’ibridazione sp3 (in questo caso) è il risultato del rimescolamento dell’orbitale 2s con i tre orbitali 2p, ottenendo così 4 nuovi orbitali identici tra loro, di forma e energia con caratteristiche intermedie rispetto agli orbitali di partenza. Gli elettroni si posizioneranno nello spazio in modo da minimizzare la loro repulsione reciproca, che in questo caso è di 109.5° orientati verso i vertici di un tetraedro. Dal mescolamento di un orbitale 2s e due orbitali p si otterranno 3 orbitali ibridi detti sp2 che si disporranno nello spazio formando angoli di 120°, geometria trigonale planare.
LEGAME C/D
I carbonio di questo legame sono ibridati sp. La combinazione (in questo caso), di un orbitale 2s e un orbitale 2p porta alla formazione di 2 nuovi orbitali ibridi che si dispongono a 180° l’uno rispetto all’altro, geometria lineare.
Uno dei tripli legami esistenti tra i due carbonio sarà di tipo sigma (quello lungo l’asse dei nuclei) i restanti due sono rispettivamente i quattro lobi degli orbitali p non ibridati che si sovrappongono sopra e sotto l’asse sigma generando due legami pigreco.
ESERCIZIO 5
1) a) singolo/singolo/doppio/triplo
b)sigma/sigma/sigma pigreco/sigma 2pigreco
c)sp3-s/sp3-s/ sp2-sp2 p-p/ sp-sp p-p p-p
d)il legame più corto è quello del carbonio d
2) a) singolo/triplo/doppio/singolo
b)sigma/sigma 2pigreco/sigma pigreco/sigma
c)sp3-s/sp-sp p-p p-p/ sp2-sp2 p-p/ sp3-s
d)il legame più corto è quello del carbonio b
ESERCIZIO 6 (A)
ESERCIZIO 7 (B)
ESERCIZIO 8 (A)
ESERCIZIO 9
a)CH3CHCHCH3
b)CH2CCCH2
c)CH2CHCCH
LikeLike